- Шкала тяжкості стану хворого панкреатитом Рансон (Ranson)
- Форми ОП (класифікація)
- стерильний панкреонекроз
- інфікований панкреонекроз
- Обстеження і моніторинг
- Лікування гострого панкреатиту
- першочергові заходи
- інфузійна терапія
- вазопресори
- знеболювання
- Заходи другої черги
- Терапія на другу добу і наступні дні
- антибіотикотерапія
- профілактики тромбоемболій
У даній статті буде розглянуто особливості лікування важкої форми гострого панкреатиту. Для встановлення діагнозу гострого панкреатиту (ОП) потрібні наявність двох будь-яких, з перерахованих нижче, критеріїв:
1. Сильний біль в епігастральній ділянці «оперізуючого характеру», з іррадіацією в спину;
2. Підвищення рівня амілази і / або ліпази в крові в 3 і більше разів вище верхньої межі норми;
3. Типові для ВП ознаки при КТ підшлункової залози з контрастним посиленням і (або) при МРТ.
Шкала тяжкості стану хворого панкреатитом Рансон (Ranson)
У ОРИТ госпіталізуються пацієнти з важким гострим панкреатитом і оцінкою по кожній із шкал: Ranson> 3, APACHE II> 8, SOFA> 3. Системи оцінки - APACHE II або шкала SOFA дозволяють найбільш об'єктивно оцінити стан хворого і передбачуваний прогноз. Але шкала Рансон більш доступна. Для полегшення грамотного написання діагнозу в історії хвороби, наводимо найбільш поширену класифікацію (м Атланта, США, 1992 р) гострого панкреатиту (в дещо скороченому вигляді).
У 2012 році вона була модернізована.
Шкала тяжкості стану хворого панкреатитом Рансон
фактор ризику
значення
вік
Старше 55 років
лейкоцитоз
Понад 16 × 109 / л
лактат дегидрогеназа
Понад 400 од / мл
аспартат трансаминаза
Більше 250 од / мл
глюкоза
Понад 11 ммоль / л
Через 48 годин:
зниження гематокриту
Більше 10%
Підйом сечовини крові
Понад 1,8 ммоль / л
Кальцій (неіонізовану)
Менше 2 ммоль / л
ВЕ
понад 4
Оціночний дефіцит рідини
Більше 6 л
РаO2
Менш 60 мм рт.ст.
Кількість факторів ризику (Кожен фактор ризику дорівнює 1 балу)
Летальність (%)
0-2
Менше 1%
3-4
≈15%
5-6
≈40%
Форми ОП (класифікація)
I. Набряковий (інтерстиціальний) ОП
II. панкреонекроз стерильний
- за характером некротичного ураження:
а) жирової
б) геморагічний
в) змішаний
- за масштабом (поширеності) ураження:
а) дрібновогнищевий
б) великовогнищевий
в) субтотальна-тотальний
- по локалізації:
а) головчасте
б) хвостовій
в) з ураженням всіх відділів ПЖ
III. інфікований панкреонекроз
ускладнення ОП
I. періпанкреатіческой інфільтрат
II. панкреатогенний абсцес
III. перитоніт:
1. ферментативний (асептичний)
2. бактеріальний
IV. Септическая флегмона заочеревинної клітковини:
V. аррозівние кровотеча
VI. механічна жовтяниця
VII. псевдокиста:
а) стерильна
б) інфікована
VIII. Внутрішні і зовнішні дігестівной свищі
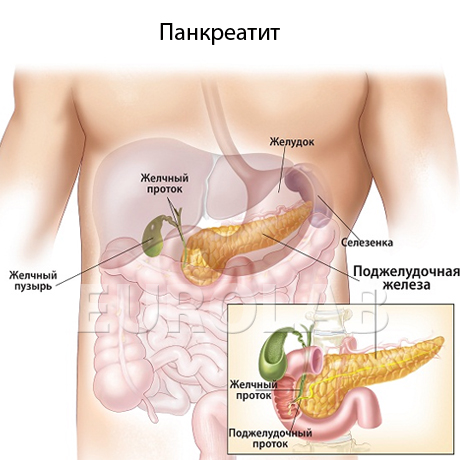
За даними різних джерел, рівень смертностіпрі важкому гострому панкреатиті (ТОП) досить висока - від 25 до 70%. До найчастішим причин ТОП зараховують жовчно-кам'яну хворобу, токсичне ураження підшлункової і організму в цілому (при прийомі алкоголю або його сурогатів), травматичні пошкодження органу. Також є ідіопатична форма ТОП, коли з якихось причин природу панкреатиту не встановили.
Морфологічним субстратом важкого гострого панкреатиту є великовогнищевий і субтотальна-тотальний панкреонекроз, якому супроводжує локальна запальна реакція (LIRS), у вигляді періпанкреатіческой інфільтрату, і системна (SIRS) запальна реакція. Як відображення цього процесу - виникнення органної дисфункції, що виявляється у вигляді панкреатогенного шоку, септичного шоку (в разі приєднання інфекції), поліорганної недостатності.
Важливим є той факт, що немає чіткого паралелізму між обсягом панкреонекрозу і ступенем органної дисфункції - дуже багато залежить від індивідуальної реакції пацієнта. Відзначимо, що при важкому гострому панкреатиті формування некрозу відбувається вже в першу добу від початку захворювання. Нагноєння некротичних мас в цей період виникає рідко.
Легеневі ускладнення - ателектаз, пневмонія, плеврит, синдром гострого легеневого пошкодження (ГРДС) - фактично маркери важкого панкреатиту. Для своєчасної діагностики потрібні повторні рентгенографические дослідження органів грудної клітини.
Протягом важкого гострого панкреатиту виділяють дві фази:
- Ранню, її тривалість менше 7 днів. Вона характеризується розвитком системної запальної реакції, що вже через 48 годин може призвести до розвитку недостатності різних органів (гострий нирковий пошкодження, ОРДС і т.д.) у частині пацієнтів.
Наявність ознак синдрому системної запальної відповіді (SIRS) говорить про тяжкість процесу і націлює на проведення активного лікування.
SIRS характеризується наявністю двох або більше критеріїв:
- ЧСС> 90 уд / хв;
- Температура тіла <36 ° C або> 38 ° C;
- Лейкоцити <4 х 109 / л або> 12 х 109 / л;
- Частота дихання> 20 за хв, або PCO2 менше 32 мм рт. ст.
- Пізню, яка розвивається в терміни> 7 днів. І характеризується розвитком місцевих ускладнень, таких як розвиток некрозу, формування помилкової кісти, абсцесу.
Якщо зона некрозу залишається стерильною, говорять про стерильному панкреонекроз, коли розвивається інфекція - це інфікований панкреонекроз.
стерильний панкреонекроз
У більшості випадків, зона некрозу залишається стерильною в перші один-два тижні від початку захворювання. Приблизно у 30-40% хворих інфікування не відбувається протягом усього захворювання.
інфікований панкреонекроз
Інфікований панкреонекроз розвивається у 40-70% пацієнтів з ТОП. Мікрофлора в зону некротичні зміни тканин проникає з товстого кишечника. Інфікований панкреонекроз слід підозрювати у пацієнтів з ТОП, чий статок погіршується, або не покращується через 7-10 днів після початку захворювання.
Пік цього процесу припадає на 10-14 день від початку захворювання. Для своєчасної діагностики, поряд з клінічними ознаками, використовується цілий ряд діагностичних прийомів (КТ або МРТ з контрастуванням, визначення прокальцитоніну і т.д.). Але «золотий стандарт» - використання тонкоголкової біопсії підшлункової залози під контролем УЗД з наступним бактеріологічним дослідженням біоптату.
І якщо ще кілька років тому саме в цей період виконувалися майже всі хірургічні втручання, то на сьогоднішній день намагаються, якщо стан хворого відносно стабільне, шляхом призначення масивної антибактеріальної терапії відстрочити проведення операції до моменту, коли відбудеться чітка демаркація зони некрозу.
А це зазвичай трапляється, коли минуло понад 4-х тижнів від моменту початку захворювання. Хворі з неінфікованим панкреонекрозу не потребують на цьому етапі в оперативному втручанні (якщо немає інших показань, наприклад - механічна жовтяниця). Вони підлягають подальшому спостереженню: іноді некротичні маси можуть повністю розсмоктуватися, в ряді випадків утворюються постнекротіческіе кісти і свищі, в рідкісних випадках - відбувається нагноєння постнекротіческіх кіст.
Обстеження і моніторинг
Типові симптоми:
- Болі в епігастрії, частіше - оперізують, що віддають в спину;
- Нудота, блювота (що не приносить полегшення);
- тахікардія .
Обстеження при надходженні
- інструментальне:
- Рентгенографія органів грудної клітки;
- УЗД черевної порожнини;
- ЕКГ за показаннями;
- лабораторне:
- Загальний аналіз крові;
- Електроліти крові;
- Креатинін крові;
- Білірубін крові;
- Загальний білок;
- Ферменти крові (АЛТ, АСТ, амілаза, ліпаза);
- Глюкоза крові;
- Лактат крові;
- Коагулограма (МНО, АЧТЧ, фібриноген, рівень D-димера);
- Гази крові - за показаннями
- Загальний аналіз сечі;
- Натрій сечі;
- Амілаза сечі.
моніторинг:
- АТ, ЦВД;
- Контроль діурезу;
- Тиск в черевній порожнині.
Лікування гострого панкреатиту
Головними цілями терапії при гострому панкреатиті є запобігання системних ускладнень захворювання, попередження інфікування при розвитку некрозу. Не вірте хірургам, коли після проведеної лапаротомії вони заявляють, що у хворого «тотальний панкреонекроз» - вони цього не можуть знати. Точно на це питання зможе відповісти патологоанатом і правильно виконана і інтерпретована КТ або МРТ підшлункової залози, та й то, мінімум, через 3 доби після початку захворювання. Якщо у хворого з ТОП виконана лапаротомія або лапароскопічне втручання з залишенням дренажів, вважайте, що ви маєте справу з інфікованим панкреонекроз.
Поліпшення результатів лікування важкого гострого панкреатиту в останні роки пов'язано не стільки з удосконаленням техніки хірургічних втручань і проведення ІТ, скільки з виробленням раціональної стратегії ведення цих хворих. Дуже важливим моментом стало розуміння того факту, що панкреонекроз, навіть інфікована, не є показанням до термінового хірургічного втручання.
Більш того, хірургічне втручання на тлі шоку значно збільшує ймовірність несприятливого результату. Операцію треба проводити: в разі важкого абдомінального компартмент-синдрому, при розвитку ускладнень ТОП - панкреатогенном абсцесі, гнійномуперитоніті, флегмони заочеревинного простору, гострої помилкової панкреатогенной кісті, прогресуючої механічної жовтяниці.
Як уже згадувалося вище, в останні роки змінилися підходи до хірургічного лікування ТОП - втручання повинно проводитися, по можливості, не раніше чотирьох тижнів після початку захворювання. Реалізація такого підходу дозволила знизити ранню летальність при ТОП. Але ці питання - зона відповідальності хірурга. На жаль, у нас в країні не так багато ЛПУ, де в змозі виконати цей «простий» алгоритм терапії.
першочергові заходи
Повинні бути розпочаті протягом першої години. До кінця першої шести годин від початку інтенсивної терапії пацієнта, бажано досягти наступних параметрів:
- Центральний венозний тиск: 80-120 мм вод. ст. Пацієнтам, яким проводиться ШВЛ, або (і) мають високу внутрішньочеревний тиск, центральний венозний тиск рекомендується підтримувати ЦВД 120-150 мм вод ст;
- ЧСС менше 110-120 уд / хв. САД> 100 мм рт. ст;
- Діурез> 0.5-1 мл / кг / год (в середньому, 60 мл / год);
- Середній артеріальний тиск: 65-85 мм рт. ст;
- Сатурація артеріальної крові за даними пульсоксиметр повинні бути більше 92%;
- Гематокрит 35-45%.
Масивний набряк підшлункової залози та інших органів черевної порожнини, іноді призводить до розвитку интраабдоминальной гіпертензії. У тих випадках, коли у пацієнта фіксують ознаки вираженої органної недостатності, резистентної до інфузії гіпотензії, терміново визначте величину тиску в черевній порожнині. Якщо має місце його підвищення понад 25-30 мм рт. ст., хворий потребує виконання негайної (протягом години) лапаротомії і накладення лапаростоми.
інфузійна терапія
Адекватна інфузійна терапія - один з найважливіших чинників в профілактиці системних ускладнень. Дефіцит рідини (блювання, плазмопотеря за рахунок накопичення рідини в черевній порожнині) часто перевищує п'ять і більше літрів. Тахікардія> 100 уд / хв майже завжди вказує на наявність гіповолемії. Вкрай важливо почати інфузійну терапію якомога раніше, використовуючи збалансовані сольові розчини (розчин Рінгер-лактат, Стерофундін та ін.). Якщо немає ниркової і серцевої недостатності, в перші 12-24 години, швидкість інфузії підтримувати на рівні 250-500 мл / год (5-10 мл / кг / год.)
Рання агресивна внутрішньовенна гідратація, з ретельним моніторингом, рекомендується всім пацієнтам, за винятком тих, у кого є супутні серцево-судинні захворювання і / або важке ниркове пошкодження. Особливу увагу слід звернути на ознаки гіпергідратації, в першу чергу такі, як набряк легенів. На тлі SIRS і високою судинної проникності, набряк легенів розвивається бурхливо, швидко приводячи до розвитку гіпоксії. На жаль, якщо пацієнт надходить для лікування не в першу добу ТОП, ефективність інфузійної терапії в плані запобігання органних порушень різко падає.
Для заповнення дефіциту рідини, особливо в разі розвитку у хворого ОРДС, олігурії, серцевої недостатності або абдомінального компартмент-синдрому, зручніше використовувати поєднання кристаллоидов і колоїдів. Це дозволяє зменшити обсяг рідини, що вводиться, прискорити відновлення перистальтики кишечника (за рахунок зменшення його набряку). Поєднання інфузії 500 мл 10% альбуміну з подальшим в / в введенням фуросеміду в дозі 1-2 мг / кг - досить ефективно працює при олігурії. Альбумін також призначають при зниженні сироватковогоальбуміну нижче 20-25 г / л або загального білка нижче 45-50 г / л. Звичайне співвідношення колоїди / кристалоїди 1: 2. Розчини глюкози на цьому етапі не використовуються (якщо немає гіпоглікемії).
Синтетичні колоїди (декстрани, ДЕК, р-р желатину) застосовувати не рекомендується - збільшують ризик розвитку гострої ниркової недостатності. Свіжозамороженої плазми для заповнення ОЦК не використовують. Звичайно, проведення інфузійної терапії - річ індивідуальна. Але добовий обсяг переливається рідини 4-5 літрів (50-70 мл / кг / добу) у хворих ТОП може бути якимсь усередненим орієнтиром.
вазопресори
До введення вазопресорів вдаються, коли, незважаючи на проведену інфузійну терапію, зберігається гіпотензія.
знеболювання
анальгетики: промедол , Морфін, фентаніл та ін. В / в, в / м - в залежності від вираженості больового синдрому. Побоювання, що введення морфіну може погіршити перебіг панкреатиту через його дії на сфінктер Одді, необгрунтовані. Трамадол часто викликає нудоту і блювоту у цих пацієнтів, тому його краще не призначати. У деяких випадках хороший аналгетичний ефект надає додаткове введення: метамізолу натрію (Анальгіну) 1-2 г 3-4 рази на добу в / в, або диклофенаку (Ортофену) 2.5% - 3.0, в / м 3 рази на добу.
Також диклофенак або індометацин призначають з метою профілактики виникнення або прогресування панкреатиту при проведенні ендоскопічної ретроградної холангіопанкреатографія (РХПГ). Правильно проведена епідуральна аналгезія забезпечує хорошу ступінь комфортності пацієнту, але вона збільшує ризик розвитку порушень центральної гемодинаміки за рахунок розвитку симпатичної блокади. Доцільність її виконання сумнівна.
Заходи другої черги
Вони можуть бути відкладені на кілька годин.
Гальмування панкреатичної секреції. Немає ніяких доказів, що застосування інгібітора протеаз апротинина (контрикал, гордокс), соматостатину, або його аналога октреотида, 5-фторурацилу в лікуванні ТОП здатне поліпшити результати захворювання.
Введення шлункового зонду. Гастропарез і застій в шлунку часто виникає у хворих з ТОП. Таким біль-ним слід встановити шлунковий зонд з метою дренування шлунка. Якщо нудоти, блювоти, застою в шлунку немає, зонд можна не ставити;
Профілактика шлунково-кишкових кровотеч. Для профілактики ерозивних ушкоджень шлунково-кишкового тракту і кровотеч призначають інгібітори протонної помпи парієтальних клітин або блокатори H2-гістамінових рецепторів.
Хоча інгібітори протонної помпи ефективніше знижують кислотність шлункового соку і менше впливають на ментальний статус хворого, блокатори H2-гістамінових рецепторів настільки ж ефективні для профілактики (зверніть увагу - але не для лікування) стрес-індукованих пошкоджень шлунка. Використовують один з перерахованих нижче препаратів. Залежно від того, чи може пацієнт приймати ентерально їжу чи ні, препарати призначають парентерально або ентерально.
Блокатори гістамінових Н2-рецепторів:
- ранітидин в / в крапельно по 50-100 мг через 8-12 годин. Всередину 150-300 мг 2-3 рази на добу;
- фамотидин в / в крапельно по 20 мг через 12 годин. Всередину з метою лікування застосовують по 10-20 мг 2 рази / добу або по 40 мг 1 раз / сут.
Інгібітори протонної помпи:
- Омепразол - внутрішньовенно крапельно в дозі 40 мг протягом 20-30 хв 1 раз на добу або всередину 20-40 мг 1 раз на добу (вміст капсули можна розжовувати);
- Езомепразол (Нексіум) вводиться внутрішньовенно в дозі 20-40 мг езомепразолу один раз на добу. Всередину 1 раз на добу по 20-40 мг. Таблетки потрібно ковтати, не розжовуючи, запивати невеликою кількістю води.
Терапія на другу добу і наступні дні
На другу добу і наступні дні, добовий обсяг інфузійної терапії обумовлений фізіологічними потребами пацієнта, зазвичай, в межах 30-35 мл / кг / добу. Іноді можливий оральний або ентеральний шлях прийому рідини.
антибіотикотерапія
інфікований панкреонекроз
Як уже було згадано вище, антибіотики можуть бути корисними в відстрочці часу хірургічного втручання, і, таким чином, можуть знизити летальність при ТОП. При панкреонекроз інфікування носить, в більшості випадків, полімікробний характер. Але частіше домінує грамотрицательная флора (Escherichia coli, Klebsiella та ін.). Вибір антибіотика полегшується, якщо виділено збудник.
Більшість антибіотиків погано проникають в тканину підшлункової залози. З цієї точки зору кращими антибактеріальними препаратами для лікування гнійних уражень підшлункової залози вважаються: карбопенеми і фторхінолони. Якщо говорити про власний досвід лікування ТОП, то комбінація ципрофлоксацину і метронідазолу виявилася не досить ефективною в лікуванні інфікованих форм панкреатиту. Кабапенеми демонстрували більш стабільні позитивні результати лікування.
В даний час препаратами вибору для проведення емпіричної терапії вважаються: Меропенем в / в 1 г через 8 годин, або Ертапем в / в 1 г на добу, або Піперацилін / тазобактам 3.375 gm в / в через 6 годин. При відсутності перерахованих лікарських засобів: Ампіцилін / сульбактам 1,5 г в \ в через 6 годин, або Тикарцилін / клавуланат 3,2 г в / в через 6 годин, або Доріпенем 1 г в / в через 8 годин. Аміноглікозиди (гентаміцин, амікацин) погано проникають в тканину підшлункової залози, але можуть застосовуватися при генералізації гнійного процесу.
Профілактичне введення антибіотиків при стерильному панкреонекроз в даний час не рекомендується. Але на практиці антибіотики, зазвичай цефалоспорини III покоління, в більшості випадків лікарі призначають - на тлі SIRS вкрай складно виключити бактеріальну інфекцію, наприклад, холангіт. Не варто використовувати для цих цілей карбапенеми і цефалоспорини IV покоління - ці препарати рекомендується залишити для лікування інфікованих форм панкреатиту, до того ж їх вартість висока. У будь-якому випадку тривалість антибиотикопрофилактики не повинна перевищувати двох тижнів. Ефективність селективної деконтамінації кишечника, як способу профілактики інфікування зони панкреонекрозу і розвитку пневмоній, не доведена.
профілактики тромбоемболій
Низькомолекулярні гепарини більш безпечні та зручні для застосування. Використовують в профілактичних дозах.
Паралітична кишкова непрохідність (паралітичний ілеус)
Дуже часто перебіг панкреатиту ускладнюється важкою динамічної кишкової непрохідності, особливо в тих випадках, коли виконувалося раннє хірургічне втручання. Зазвичай, паралітична кишкова непрохідність дозволяється самостійно через 2-4 доби. Прискорити цей процес допомагають такі прийоми:
Ретельно відкоригуйте електроліти крові. Якщо має місце значна (<25 г / л) гіпоальбумінемія - усуньте її. Справа в тому, що при зниженні рівня альбуміну розвивається набряк кишки, і вона погано скорочується. Намагаються усунути гіпергідратацію, яка також викликає набряк внутрішніх органів і кишечника. Для чого можна призначити фуросемід в дозі 0,5-1 мг / кг в / в.
Блокатор периферичних і центральних дофамінових рецепторів метоклопрамид (Церукал) підвищує рухову активність початкового відрізка тонкої кишки і сприяє усуненню дуодено-гастрального рефлюксу, покращує евакуацію їжі зі шлунка. Метоклопрамід вводять в / в по 10-20 мг, 2-3 рази на добу. У разі збереження стійкого парезу кишечника більше 3-х діб, використовують введення антихолінестеразних препаратів: 1-2 мг п / к неостигміну (прозерин) два-три рази на добу.
нутритивная підтримка
На сьогоднішній день вважається доведеним, що найкращі результати в плані результатів захворювання забезпечує раннє (з другої доби захворювання) ентеральне харчування, так як воно може зменшити число гнійних ускладнень шляхом підтримки бар'єрної функції кишечника і знизити ймовірність бактеріальної транслокації з кишечника в зону некрозу.
Однак часто парез шлунка у хворих з ТОП зберігається тривалий час, і годування пацієнта через назогастральний зонд в перші кілька діб захворювання неможливо. Було показано, що евакуаторної здатність тонкої кишки при панкреатитах страждає слабо. У зв'язку з цим, більш ефективним методом годування хворого, вважають проведення ентерального харчування через назоеюнальний зонд, встановлений дистальніше зв'язки Трейца ендоскопічним шляхом або під час операції. На жаль, технічні складності з проведенням зонда в тонку кишку, обмежують застосування цієї методики.
Зазвичай використовують стандартні ентеральні суміші, краще безлактозние (немолочні), ізокалоріческіе (1 ккал / мл), ізонітрогенние (35-45г білка в 1 л). Орієнтовна добова енергетична потреба - 25-35 ккал / кг. Краще безперервний спосіб введення поживних сумішей в зонд. У першу добу суміш вводять зі швидкістю 25 мл / год. Потім, якщо пацієнт добре справляється із зазначеним об'ємом, швидкість введення поступово, протягом 2-3 діб, збільшують.
У разі розвитку непереносимості ентерального харчування (збільшення рівнів амілази і ліпази в крові, стійкий парез кишечника, діарея, аспірація) або неможливості установки назоеюнального зонда, показано проведення парентерального. Зазвичай його починають не раніше 5 діб від моменту захворювання.
Нам здається, що для цих цілей найбільш зручно використовувати комплексні препарати для парентерального харчування, що містять в одній упаковці всі необхідні нутрієнти (наприклад, ОліКліномель). Але частота ускладнень, в першу чергу, інфекційних, при парентеральному харчуванні вище, ніж при ентеральному.
Гіперглікемія. У деяких хворих, в результаті руйнування острівцевих клітин, може різко підвищитися рівень глюкози в крові. У цих випадках гіперглікемія коригується введенням простого інсуліну.
Екстракорпоральних методів детоксикації (гемодіаліз, гемофільтрація і ін.) Використовують при прогресуванні ниркової недостатності, яка не піддається консервативному лікуванню.

