- Причини виникнення токсоплазмозу
- Як лікувати токсоплазмоз?
- З якими захворюваннями може бути пов'язано
- Лікування токсоплазмозу в домашніх умовах
- Якими препаратами лікуваті токсоплазмоз?
- Лікування токсоплазмозу народними методами
- Лікування токсоплазмозу під час вагітності
- До яких лікарів звертатися, якщо у Вас токсоплазмоз
- Лікування інших захворювань на букву - т
Причини виникнення токсоплазмозу
токсоплазмоз - зоонозное протозойне захворювання, відноситься до групи TORCH-інфекцій, що викликаються внутрішньоклітинним паразитом Toxoplasma gondii, яке в разі манифестного течії характеризується поліморфізмом клінічних проявів з переважним ураженням нервової, лімфатичної систем, очей, скелетних м'язів і міокарда.
Актуальність проблеми токсоплазмозу обумовлена високою сприйнятливістю людини до зараження токсоплазмами, значним поширенням інвазії серед населення земної кулі (20-30%), приналежності хвороби до TORCH-комплексу, розвитком важких маніфестних форм у пацієнтів з імуносупресією, неможливістю досягти санації макроорганізму за допомогою відомих на сьогодні препаратів (так як вони не діють на цисти - основну форму існування токсоплазм в організмі людини), обмеженістю сучасних методів підтвердження зв і наявності в організмі людини токсоплазм з клінічними проявами. Існує більше 20 методів специфічних досліджень при токсоплазмозі, але жоден з них не задовольняє повністю потреб медицини.
Збудник токсоплазмозу відноситься до роду Toxoplasma, сім'ї Eimeriidae, підцарства Protozoa. Це умовно-патогенний внутрішньоклітинний паразит, який існує в трьох формах: тахізоіти (трофозоїти), брадізоіти (цисти) і спорозоїти (ооцисти). Тахізоіти нагадують за формою півмісяць, а при фарбуванні за Романовським-Гімзою цитоплазма набуває блакитно-сірий, а ядро - червоно-фіолетовий забарвлення. Тип руху - ковзний. Розмножуються внутрішньоклітинно шляхом поздовжнього поділу і внутрішнього брунькування в організмі ссавців, в тому числі і людини, і птахів, утворюючи псевдоцисти (акумулюють по 8-16 паразитів всередині клітини), які з'являються в тканинах в гострій стадії.
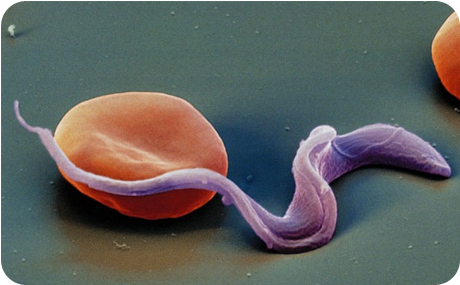
Тахізоіти високочутливі до термічних, фізичних і хімічних агентів.
Брадізоіти існують у вигляді справжніх цист ланцетовидной форми (мають власну оболонку, всередині якої розташовані кілька тисяч брадізоітов), можуть перебувати в будь-якому органі, але найчастіше в скелетних м'язах, печінці, міокарді, ЦНС, викликаючи хронічний перебіг інфекції. Цисти стійкі до різного роду впливів, в тому числі і хіміопрепаратів.
Спорозоїти (ооцисти) мають овальну форму, утворюються тільки в клітинах слизової оболонки кишечника представників сімейства котячих, виводяться з випорожненнями назовні. Ооцисти є стійкими до впливу чинників навколишнього середовища, при цьому вони здатні зберігати життєздатність і інвазивність протягом 1,5-2 років через споруляцію, яка відбувається протягом 1-5 днів після виходу з організму котячих. Після цього ооцисти містять по 2 спороцисти, кожна з них має 4 спорозоїти.
Життєвий цикл збудника проходить зі зміною двох стадій:
- безстатевою (шизогонія) - в клітинах різних тканин багатьох проміжних господарів (ссавців, птахів, людини),
- статевої (гаметогонія) - виключно в епітелії кишок основного господаря (представників сімейства котячих).
При безстатевої стадії проміжний господар заковтує спорулірованние ооцисти паразита, що містять спорозоїтів, або цисти, що містять брадізоітов. Під дією кислого вмісту шлунка оболонка ооцист і цист швидко руйнується. Спорозоїти і брадізоіти, що вийшли з них, занурюються в епітелій тонкої кишки і перетворюються в ендозоіти - форми паразита, які швидко діляться і здатні розмножуватися в будь-яких клітинах ссавців, крім еритроцитів. Паразит прикріплюється до клітини і проникає в неї, утворюючи паразітофорную вакуоль, усередині якої ділиться. Розмноження триває, поки кількість ендозоіти не перевищить можливості клітини - в кінці кінців вона лопається, а паразити проникають в сусідні клітини. Більшість ендозоіти гинуть завдяки гуморального і клітинного імунної відповіді.
Через 7-10 діб після дисемінації інфекції в тканинах утворюються цисти, що містять безліч брадізоітов. Цисти можуть зберігатися до кінця життя проміжного господаря. На цьому безстатева стадія циклу розвитку паразита завершується.
Статева стадія протікає в організмі представників сімейства котячих і характеризується утворенням ооцист. Від проміжного господаря (птиці і гризуни, які служать здобиччю для кішок) цисти потрапляють в організм основного господаря. Брадізоіти прикріплюються до слизистого епітелію кишок і проходять там кілька проміжних стадій розвитку. Процес закінчується утворенням гамет. Після злиття гамет утворюється зигота, оточена міцною оболонкою, яка виділяється з випорожненнями у вигляді неспорулірованной ооцисти. Ця форма паразита для людини безпечна. Але через деякий час перебування в навколишньому середовищі вона стає спорулірованной. Коли спорулірованние ооцисти заковтує проміжний господар, цикл починається спочатку.
Токсоплазмоз - убіквітарний зооноз, тобто основним джерелом інфекції є домашні і дикі ссавці. Хвора людина при будь-якій формі токсоплазмозу не заразний для оточуючих. Винятком є лише вагітна, хвора на гострий токсоплазмоз, яка може внутрішньоутробно інфікувати плід, і в деяких випадках - донори крові і тканин.
Існують наступні шляхи зараження токсоплазмозом:
- пероральний - 97% всіх випадків зараження; при споживанні сирих продуктів, вироблених з м'яса великої та дрібної рогатої худоби; факторами передачі можуть бути брудні руки, продукти харчування, вода, посуд, контаміновані ооцистами;
- контактний - 1% всіх випадків зараження, при пошкодженні шкіри або слизових оболонок і внесення в рани спорулірованних ооцист;
- вертикальний - 1% всіх випадків зараження, в разі виникнення у жінки під час вагітності паразитемии;
- ятрогенний - 1% всіх випадків зараження; реалізується при переливанні крові та трансплантації органів.
Інфікованість токсоплазмами широко поширена у всіх країнах земної кулі і варіює від 5-10% до 50-80% в залежності від віку, національних особливостей, санітарно-гігієнічного рівня населення. Жінки інфікуються в 2-3 рази частіше, ніж чоловіки.
Сприйнятливість до токсоплазмозу висока. Імунітет при токсоплазмозі нестерильний, інфекційний. Імунний стан зберігається при наявності в організмі збудника, найчастіше у вигляді цист. Антигенні метаболіти, які продукують цисти, підтримують певний рівень гуморального імунітету, а також обумовлюють розвиток гіперчутливості сповільненого типу.
З місця проникнення (найчастіше через травний канал) токсоплазми з струмом лімфи потрапляють в регіонарні лімфатичні вузли, де вони розмножуються і викликають розвиток лімфаденіту. Потім паразити у великій кількості надходять в кров і розносяться по всьому організму, викликаючи ураження ЦНС, печінки, селезінки, лімфатичних вузлів, скелетних м'язів, міокарда, очей. Внаслідок розмноження паразитів руйнуються заражені клітини. Навколо вогнищ некрозу і скупчення токсоплазм утворюються специфічні гранульоми. В результаті життєдіяльності паразита і виділення антигенів відбуваються алергічна перебудова організму за типом реакцій гіперчутливості уповільненої типу і синтез специфічних антитіл. Наявність антитіл запобігає нове зараження навіть високовірулентних штамами токсоплазм і обумовлює латентний перебіг токсоплазмозу у більшості інвазованих осіб. У деяких випадках виникають тромбоваскуліти з вогнищами асептичного некрозу. При розсмоктуванні останніх утворюються множинні порожнини - кісти. Спостерігають ізвествленіе вогнищ запалення з утворенням розсіяних кальцификатов. У разі важких придбаних форм токсоплазмозу виявляють анемію, крововиливи в серозні оболонки, дилатацію порожнин серця, набряк легенів, некротичні вогнища в печінці, селезінці, набухання лімфатичних вузлів, повнокров'я головного мозку. У хворих з нормальним імунітетом розвиток інфекції стримують гуморальний і клітинний імунну відповіді. Знищення ендозоіти відбувається за допомогою декількох механізмів - освіту антипаразитарних антитіл, активація макрофагів, синтез інтерферону і стимуляція цитотоксичних Т-лімфоцитів. Ці антигенспецифической лімфоцити знищують як позаклітинні форми паразитів, так і уражені токсоплазмами клітини. У хворих з ослабленим імунітетом рецидиви токсоплазмозу, ймовірно, обумовлені виходом брадізоітов з цист і швидким перетворенням їх в ендозоіти безпосередньо в ЦНС. У міру знищення ендозоіти в тканинах (зазвичай в ЦНС і сітківці очей) починають утворюватися цисти. Захворювання з гострої фази переходить в хронічну, а частіше - в хронічну з бактеріоносійство. Механізми, які перешкоджають розвитку інфекції, не спрацьовують при імунодефіциті і під час внутрішньоутробного розвитку. При природженому токсоплазмозі відбувається недорозвинення півкуль головного мозку. Поразка епендими, виникнення спайок в шлуночках мозку і облітерація субарахноїдальних просторів призводять до розвитку гідроцефалії. При пізньої фетопагіі в корі великого мозку, подкорковой області і стовбурі з'являються вогнища некрозу і кальцифікації. Характерно продуктивне запалення речовини головного мозку і його оболонок, тобто розвивається менінгоенцефаліт. Вогнища некробіоза виникають в сітківці очей з утворенням гранульом в судинному тракті (продуктивно-некротичний ендофтальміт).
Міжнародна класифікація хвороб виділяє наступні клінічні форми токсоплазмозу:
- токсоплазмозний хориоретинит;
- токсоплазмозний гепатит;
- токсоплазмозний менінгоенцефаліт;
- легеневий токсоплазмоз;
- токсоплазмоз з ураженням інших органів (міокардит, міозит);
- токсоплазмоз неуточнений.
Залежно від клінічних проявів більшість фахівців розрізняють:
- придбаний токсоплазмоз (до 99% всіх випадків зараження Т. gondii, зазвичай має безсимптомний перебіг);
- вроджений токсоплазмоз.
За характером перебігу манифестного токсоплазмозу виділяють:
- гострий токсоплазмоз (до 0,01% інфікованих);
- хронічний токсоплазмоз (1-5%), має схильність до рецидивів і загострень.
При гострому прояві токсоплазмозу загальними інтоксикаційними симптомами є:
- Загальна слабкість,
- головний біль,
- нездужання,
- підвищення температури тіла,
- міалгія,
- артралгія.
Внаслідок порушення імунного статусу може відбуватися генералізація токсоплазмозу:
- підвищення температури тіла до 39-40 ° С,
- збільшення лімфатичних вузлів,
- збільшення печінки з можливим ураженням інших органів і систем.
У разі мононуклеозоподібних течії токсоплазмозу спостерігають:
- виражене збільшення шийних, потиличних, пахових, пахвових лімфатичних вузлів,
- лімфомонопітоз,
- незначну еозинофілію,
- тривалий субфебрилітет.
У разі екзантемную течії токсоплазмозу провідними симптомами є:
- висип,
- збільшення лімфатичних вузлів,
- підвищення температури тіла,
- ознаки міокардиту,
- ендокардиту,
- енцефаліту (частіше у дітей і осіб похилого віку).
У разі гастроентероколічного течії токсоплазмозу розвиваються:
- незначні диспепсичні симптоми,
- мезаденит,
- рідше гепатит,
- підвищення температури тіла,
- збільшення печінки,
- збільшення лімфатичних вузлів.
Менінгоенцефаліческое перебіг токсоплазмозу проявляється:
- вираженим серозним менінгітом,
- ознаками ураження речовини мозку,
- можливо переважання симптомів міокардиту,
- можливо переважання симптомів міокардитичного кардіосклерозу без розвитку пороку серця.
При ураженні очей (хоріоретиніт, увеїт) може розвинутися сліпота.
Хронічний перебіг має три основні варіанти:
- частіше спостерігають лише наростання титру антитіл в динаміці, без клінічних проявів (абортивний варіант);
- неспецифічний варіант проявляється головним болем, помірним нездужанням, збільшенням лімфатичних вузлів, стійким субфебрилитетом, випаданням волосся;
- для клінічно вираженого варіанту характерний поліморфізм проявів з боку всіх органів і систем; в більшості випадків виявляють лімфаденонатію, міозити, артралгії, міокардит або міокардіодистрофію, можливі пневмоніт, гастрит, ентероколіт, ураження жовчних шляхів і жіночої статевої системи (порушення менструального циклу, сальпінгоофорит, ендометрит, безплідність).
Важливу роль відіграє ураження нервової системи: головного мозку, його оболонок, гіпоталамуса, периферичних нервів; проявляється менінгоенцефаліт, енцефаліт, ураження судин, вегетативні і психічні розлади, судомний синдром. При ураженні очей можливі патологічні зміни в усіх оболонках, виникають пошкодження зорового нерва, зовнішніх м'язів очного яблука. У поєднанні з хоріоретінітом і іншими проявами іноді відзначають кератосклеріт або кератоувеїти.
У осіб з імунодефіцитними станами латентний перебіг або нове зараження переходить в генералізований процес з ураженням головного мозку, міокарда, легень і інших органів і тканин. Найчастіше уражається ЦНС - виникає важкий некротичний енцефаліт. У різних країнах мозкову локалізацію токсоплазмозу виявляють у 3-40% хворих на СНІД. У клінічній картині переважають симптоми вогнищевого енцефаліту, що вказує на ураження півкуль великого мозку, мозочка або стовбура (геміпарез, афазія, дезорієнтація, гемианопсия, судомний синдром і ін.), Які часто поєднуються з енцефалопатією.
Позамозкова локалізація токсоплазмозу при СНІДі характеризується переважно ураженням очей (50%), яке проявляється вогнищевим некротическим хоріоретінітом без запальної реакції; можуть залучатися і інші органи (серце, легені, лімфатичні вузли, кістковий мозок, печінка, підшлункова залоза, сечова і статева системи).
Як лікувати токсоплазмоз?
Протипаразитарне лікування токсоплазмозу безперечно показано:
- при маніфестному гострому розвитку інфекції,
- при хронічному розвитку в період загострення,
- в разі набутого токсоплазмозу при наявності хориоретинита,
- на тлі невиношування вагітності, безпліддя.
Для лікування токсоплазмозу у імунокомпетентних осіб при відсутності вагітності призначають:
- доксициклін - по 0,1 г 2 рази на добу всередину протягом 10 днів;
- хлорохин - по 0,25 г 3 рази на добу в поєднанні з метронідазолом по 0,2 г 3 рази на добу протягом 7-10 днів;
- комплекс піріметаміну з сульфадоксину по 1 таблетці 2 рази на добу протягом 5 днів з перервою в 5-7 днів, під час якого рекомендують вживати препарати фолієвої кислоти, а потім повторити курс сульфадоксину.
Протягом усієї етіотропної терапії призначають десенсибілізуючі і симптоматичні засоби.
Для лікування осіб з імунодефіцитом при відсутності вагітності одночасно призначають не менше двох препаратів антипротозойної дії. Кожні 10 діб проводять заміну одного або двох препаратів. Крім вищеназваних засобів можливо пероральне призначення кліндаміцину або спіраміцину. Обов'язково застосовують глюкокортикоїди, препарати фолієвої кислоти, дегидратационную і дезінтоксикаційну терапію.
При ВІЛ-інфекції призначають ті ж препарати протягом 3-6 тижнів. Надалі рекомендується довічна профілактика рецидивів.
Одноразовий курс комплексної терапії вважається ефективним в 90% випадків; другий курс можна проводити з 30-го тижня вагітності. Хворі латентним хронічним токсоплазмозом не потребують специфічному антипротозойним лікуванні; їм показана традиційна терапія супутніх захворювань.
Лікування токсоплазмозу в період загострення має бути комплексним. Тривала антипротозойним терапія патогенетично не обгрунтована. Лікування супутніх захворювань, санацію вогнищ хронічних інфекцій, які негативно впливають на стан імунної системи, бажано проводити до призначення антипротозойних препаратів.
З якими захворюваннями може бути пов'язано
У разі пріобретеннго токсоплазмозу характерними ускладненнями стають:
- кардіосклероз з розвитком серцево-судинної недостатності,
- наслідки енцефаліту, крововиливи в речовину мозку,
- приєднання вторинної інфекції.
У разі вродженого токсоплазмозу відбуваються такі ускладнення як:
- затримка фізичного і психічного розвитку,
- парези і паралічі,
- сліпота,
- глухота.
При розвитку набутого токсоплазмозу на тлі імунодефіциту і в разі важкого вродженого токсоплазмозу прогноз дня життя вкрай несприятливий.
Лікування токсоплазмозу в домашніх умовах
Лікування токсоплазмозу в домашніх умовах не володіє достатньою ефективністю, хоч прийом призначених лікарем препаратів на певному етапі і може проводитися на дому. Пацієнт з характерними симптомами зазвичай піддається госпіталізації в інфекційне відділення, адже тут він виявляється під контролем профільних фахівців.
Якими препаратами лікуваті токсоплазмоз?
- доксіціклін - по 0,1 г 2 рази на добу всередину в течение 10 днів;
- кліндаміцін - по 0,45 г 3 рази на добу;
- піріметамін - по 1 таблетці 2 рази на добу протягом 5 днів з перервою в 5-7 днів, під час якого рекомендують вживати препарати фолієвої кислоти;
- Спіраміцин - по 1 г 3 рази на добу;
- хлорохін - по 0,25 г 3 рази на добу протягом 7-10 днів;
- метронідазол - на додаток до хлорохіну по 0,2 г 3 рази на добу протягом 7-10 днів.
Лікування токсоплазмозу народними методами
Лікування токсоплазмозу народними засобами не здатне надати достатнього дії на спровокувала захворювання інфекцію, а тому вважається марним затягуванням часу. Розвиток характерних для захворювання симптомів повинно бути приводом для звернення до профільного медичного закладу за наданням професійної допомоги.
Лікування токсоплазмозу під час вагітності
Особливістю токсоплазмозу у вагітних є переважно безсимптомний перебіг, тому діагностувати первинне інфікування або загострення хронічного токсоплазмозу можна тільки на підставі результатів лабораторних досліджень, проведених в динаміці. За сучасними уявленнями, внутрішньоутробне зараження плода відбувається трансплацентарно від матері, хворої на активну форму токсоплазмозу, в разі гострого розвитку інфекції або інфікування протягом 6 місяців перед початком вагітності.
Первинне інфікування вагітних може закінчитися мимовільним викиднем, передчасними пологами, мертвонародження, народженням живого інфіковану дитину. Розвиток вродженого токсоплазмозу можливо тільки при первинному зараженні токсоплазмами під час вагітності, його частота становить 1 випадок на 1000-3500 народжених дітей. Залежно від часу інфікування плода розрізняють:
- хронічний перебіг (небезпечно, зараження відбувається в I триместрі вагітності), яке характеризується вадами розвитку мозку (атрофія, гідроцефалія, деформація шлуночків мозку), очей (анофтальмия, колобома, атрофія сітківки), можливі вади розвитку інших органів;
- підгострий перебіг (інфікування в II триместрі), проявляється активним енцефалітом, менінгоенцефалітом в поєднанні з ураженням очей у вигляді вогнищевих некрозів і запалення сітківки (хоріоретиніт, увеїт);
- гострий перебіг (інфікування в III триместрі), при якому підвищується температура тіла, виникають плямисто-папульозний висип, жовтяниця, гепатоспленомегалія, анемія, міокардит, пневмонія, ураження кишечника.
У деяких випадках гострота процесу стихає; у хворих спостерігають общеінтоксікаціонного симптоми, які періодично посилюються, ознаки ураження ЦНС і органу зору (затримка психомоторного розвитку, парези, паралічі, епілептиформні припадки, хоріоретиніт). При відсутності ознак тривалого інвазивного процесу можуть зберігатися стійкі необоротні зміни (мікроцефалія, кальцинати в головному мозку, часткова атрофія зорових нервів, хоріоретинальні рубці), які слід трактувати як залишкові симптоми. У віці 10-12 років можливо гострий перебіг з субклиническими проявами. У деяких випадках також виявляють затримку фізичного та психічного розвитку, епілептиформні припадки, ендокринні розлади, хоріоретиніт.
Лікування гострого токсоплазмозу у вагітних переслідує дві мети:
- санація токсоплазмозу у матері,
- профілактика токсоплазмозу.
Після 16-го тижня вагітності призначають спирамицин всередину по одній з нижче наведених схем (визначає лікуючий лікар):
- разова доза 1,5 г двічі на добу протягом 6 тижнів;
- разова доза 3 г двічі на добу протягом 4 тижнів;
- разова доза 3 тричі на добу протягом 10 днів.
З 12-13-го тижня вагітності, а також в разі призначення спіраміцину проводять імунотерапію імуноглобуліном людини проти Т. gondii, що показано при лікуванні токсоплазмозу у вагітних та урогенітальної патології на тлі токсоплазмозу. Імуноглобулін вводять одночасно з антигістамінними препаратами, які можна застосовувати під час вагітності.
Вибір схеми лікування є суто індивідуальним, її призначає лікар-інфекціоніст, який володіє вибраною методикою терапії.
Профілактика токсоплазмозу включає ретельну термічну обробку продуктів харчування, особливо м'ясних продуктів і молока, дотримання правил особистої гігієни, запобігання забрудненню місць перебування та ігор дітей екскрементами кішок. Основними заходами профілактики токсоплазмозу є своєчасне обстеження жінок репродуктивного віку та вагітних в жіночих консультаціях.
До яких лікарів звертатися, якщо у Вас токсоплазмоз
У загальних лабораторних дослідженнях порушення відповідають конкретної клінічної ситуації і не мають характерних саме для токсоплазмозу змін, інструментальні методи використовують для виявлення неспецифічних, але притаманних для токсоплазмозу ознак (КТ, МРТ головного мозку, в тому числі з судинної контрастною програмою, УЗД, ЕКГ, офтальмоскопія ).
Показаннями до обстеження на токсоплазмоз є:
- вагітність, підозра на вроджений токсоплазмоз (але перше обстеження доцільно проводити на етапі планування сім'ї);
- стійке невиношування вагітності, безпліддя;
- тривале (більше 3 тижнів) підвищення температури тіла до субфебрильних цифр невстановленого походження;
- збільшення периферичних лімфатичних вузлів (шийних, потиличних, пахвових, ліктьових), якщо воно не може бути пояснено іншими причинами;
- повільне прогресування нейроінфекції в поєднанні з лімфаденітом, збільшенням печінки, селезінки, приєднанням ураження органу зору і міокардиту з 3-го тижня захворювання;
- ураження ока (хоріоретиніт), що супроводжуються субфебрилитетом, збільшенням лімфатичних вузлів, печінки, селезінки, болем у м'язах і суглобах.
Поліморфізм клінічних проявів як придбаного, так і вродженого токсоплазмозу, відсутність патогномонічних симптомів обумовлює необхідність ретельного підтвердження діагнозу з використанням специфічних методів лабораторних досліджень. Переважна більшість фахівців визнають, що ні один окремо взятий метод дослідження не може повністю вирішити проблему діагностики токсоплазмозу. У нормі токсоплазми можна виявити у 30% клінічно здорових осіб. Тому (з огляду на багаторічну персистенцию збудника) виявлення IgG до токсоплазм в будь-яких концентраціях є лише констатацією факту наявності Т. gondii в організмі обстежуваного. Виділяють наступні методи специфічної діагностики:
- паразитологічний метод - виявлення збудника при мікроскопії мазків крові, спинномозковій рідині, навколоплідних вод, плаценти, абортивного матеріалу, який помер плода або дитини; існує ряд недоліків, істотно знижують його цінність і, відповідно, обмежують застосування на практиці; більше значення має виявлення трофозоітов, розташованих внеклеточно, що вказує на активне розмноження збудника;
- серологічні методи - дозволяють підтвердити наявність специфічних антитіл в сироватці крові, спинномозковій рідині, навколоплідних водах; найбільш достовірним і специфічним вважають ІФА, яким здійснюється не тільки виявлення антитіл до токсоплазм різних класів, але і визначення їх концентрації;
- ПЛР - виявлення ДНК токсоплазм в матеріалі, взятому у хворого (амніотична рідина, пуповинна кров, спинномозкова рідина);
- біопсія лімфатичних вузлів і биопроба на тварин (ці методи рідко застосовують у розвинених країнах).
У хворих з нормальним імунітетом виявлення IgM і наростання його титру через 3 тижні в сироватці хворого свідчить про гострому розвитку набутого токсоплазмозу. Наростання титру IgG без збільшення концентрації IgM вказує на хронічне розвиток токсоплазмозу.
У ВІЛ-інфікованих основою для передбачуваного діагнозу токсоплазмозу служить виявлення в сироватці IgG і характерних змін при КТ і МРТ голови. Спроби виявити IgM або наростання титру IgG в цьому випадку є безпідставними. Підтвердженням діагнозу може бути виявлення антитіл за допомогою ІФА, а також ДНК паразита за допомогою ПЛР у спинномозковій рідині. Для пренатальної діагностики вродженого токсоплазмозу використовують кордоцентез і амніоцентез з подальшим визначенням IgM і проведенням біопроби на мишах. Також за допомогою ПЛР виявляють ген В1 паразита в навколоплідних водах.
У новонароджених серодиагностика грунтується на зберіганні IgG протягом тривалого часу і виявленні IgM через тиждень після народження. Титр IgG оцінюються кожні 2 місяці. Наростання титру IgM після 1-го тижня життя вказує на гострий перебіг токсоплазмозу. Однак до 25% новонароджених залишаються серонегативними і не мають відхилень при огляді, тому для встановлення діагнозу необхідні КТ, МРТ, офтальмологічне обстеження, специфічні дослідження спинномозкової рідини.
Критерії, що дозволяють виключити діагноз токсоплазмозу:
- негативні серологічні реакції (відсутність специфічних антитіл до Т. gondii класів IgM, IgG за допомогою ІФА) на тлі помірного імунодефіциту;
- негативні серологічні реакції, виконані з інтервалом 2-3 тижні, навіть при наявності деяких підозрілих клінічних ознак, роблять діагноз токсоплазмозу вкрай малоймовірним;
- виявлення специфічних IgG до Т. gondii без клінічних проявів токсоплазмозу не може служити підставою для діагностування маніфестних форм хвороби і призначення етіотропної терапії.
Лікування інших захворювань на букву - т
Інформація призначена виключно для освітніх цілей. Не займайтеся самолікуванням; з усіх питань, які стосуються визначення захворювання і способів його лікування, звертайтеся до лікаря. EUROLAB не несе відповідальності за наслідки, спричинені використанням розміщеної на порталі інформації.
Як лікувати токсоплазмоз?
Якими препаратами лікуваті токсоплазмоз?

