- Нова парадигма: серцево-судинний континуум.
- Короткі і довгі шляхи серцево-судинного континууму.
- Порочне коло в серцево-судинному континуумі.
- Фактори ризику.
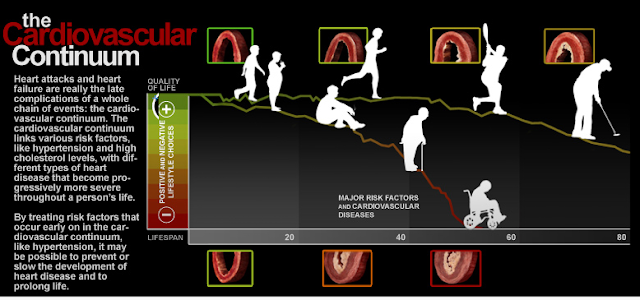
Нова парадигма: серцево-судинний континуум.
З давніх-давен було відомо, що ожиріння часто поєднується з такими захворюваннями, як ішемічна хвороба серця, артеріальна гіпертензія, інфаркти, інсульти, атерогенная дислипидемия, ЦД 2 типу, подагра, безпліддя, полікістоз яєчників, «венозний тромбоемболізм», «нічний апное» і ін. Подання про зв'язок надлишку жирової тканини з серцево-судинними захворюваннями з'явилося понад півстоліття тому. Відомий клініцист Е.М. Тареев в 1948 р писав: «Уявлення про гіпертоніків найбільш часто асоціюється з ожирел гіперстенік, з можливим порушенням білкового обміну, із засміченням крові продуктами неповного метаморфоза - холестерину, сечової кислоти ...»
У 1991 році Dzau і Braunwald запропонували концепцію серцево-судинного континууму (cardiovascular continuum), що представляє собою ланцюг послідовних подій, що призводять в фіналі до розвитку застійної серцевої недостатності і смерті хворого. Пусковими ланками цього «фатального каскаду» є серцево-судинні фактори ризику, артеріальна гіпертонія (АГ), а також цукровий діабет. Багато помиляються, думаючи, що інфаркти та інсульти трапляються раптово, насправді все зумовлюється ще в молодості. Розуміння даної концепції дозволить більш усвідомлено підійти до лікування та профілактики серцево-судинних захворювань.
Серцево-судинний континуум - єдиний механізм дерегуляції, що включає всі патофізіологічні процеси, що призводять від факторів ризику до хвороби, ремоделированию, дилатації лівого шлуночка, формування ХСН (хронічної серцевої недостатності) і смерті. Суть феномена полягає в тому, що такі фактори ризику як АГ, цукровий діабет, дисліпідемія, через гіпертрофію і дилатацію лівого шлуночка, або через розвиток атеросклерозу, ІХС, гострого інфаркту міокарда призводять до загибелі і глибокого сну кардіоміоцитів, активації тканинних та циркулюючих нейрогормонів і в результаті до ремоделированию серця і формування ХСН.
У свою чергу, хронічна серцева недостатність призводить або до смерті від наростаючої декомпенсації, або через життєво небезпечні тахи- і брадиаритмии до раптової смерті таких важко хворих. Важливою особливістю серцево-судинного континууму є те, що з певного етапу ураження серця прогресування ХСН відбувається за загальними закономірностями, практично не залежних від етіології захворювання.
У прогресуванні дисфункції і ремоделировании міокарда при ССЗ і ХСН (хронічна серцева недостатність) значна роль належить підвищенню активності таких нейрогормональних систем, як СНС і РААС.
Ще А.Л. М'ясників в 1965 р в монографії «Гіпертонічна хвороба і атеросклероз» підкреслював, що «поєднання гіпертонічної хвороби з атеросклерозом і пов'язаної з ним коронарною недостатністю настільки часто зустрічається в практиці і так переважає над« чистими »формами, що виникає задача розглядати ці патологічні стани не тільки в їх типовому ізольованому вигляді, але і в часто зустрічається комплексі ». Мета-аналіз MacMahon et al., Заснований на результатах 9 проспективних досліджень, які включили в цілому більше 400000 хворих, ще раз підтвердив, що ймовірність розвитку ішемічної хвороби серця (ІХС) знаходиться в прямій лінійній залежності від рівня як систолічного (САТ), так і діастолічного (ДАТ) АТ.
Крім того, АГ є найважливішим прогностичним фактором інфаркту міокарда (ІМ), гострого і минущого порушення мозкового кровообігу, хронічної серцевої недостатності, загальної та серцево-судинної смертності. У свою чергу, наявність у хворого з АГ ІХС, незалежно від її форми (стенокардія напруги, інфаркт міокарда, перенесена операція реваскуляризації міокарда) може розглядатися як «супутнє клінічний стан», в значній мірі впливає на загальний серцево-судинний ризик пацієнта. Міжнародне Товариство з Артеріальною Гіпертензії і Європейське Співтовариство кардіологів (ISH / ESC) рекомендує відносити хворого, який страждає одночасно ГБ і ІХС, до групи дуже високого ризику.
Взаємозв'язок між АГ і ІХС цілком з'ясовна. По-перше, обидва захворювання мають однакові фактори ризику, по-друге, механізми виникнення і еволюції АГ і ІХС багато в чому схожі. Так, вважається загальновизнаною роль ендотеліальної дисфункції (ЕД) в розвитку як АГ, так і ІХС.
Дисбаланс між прессорной і депрессорной системами регуляції тонусу судин викликає на початкових етапах підвищення рівня артеріального тиску, а згодом стимулює процеси ремоделювання серцево-судинної системи, що зачіпають лівий шлуночок, магістральні і регіонарні судини, а також мікроциркуляторного русла. На рівні коронарних артерій ЕД стимулює атерогенез, що приводить до формування, а в кінцевому підсумку, до дестабілізації бляшки, її розриву й розвитку інфаркту міокарда (ІМ).
Особливий інтерес викликає той факт, що порушення ендотелій-залежної регуляції тонусу коронарних артерій створюють додатковий динамічний стеноз до вже наявного анатомічному.
Короткі і довгі шляхи серцево-судинного континууму.
визначають серцево-судинний континуум наступним чином - це безперервний розвиток серцево-судинних захворювань - від факторів ризику до загибелі хворого. Континуум можна проходити швидко або повільно. Існують більш довгі і більш короткі шляхи від появи чинників ризику до летального результату. Складний пацієнт, швидко проходить серцево-судинний континуум, вмирає рано.
1. Пусковий момент.
Пусковим моментом серцево-судинного континууму є артеріальна гіпертензія, цукровий діабет, дисліпідемія, ожиріння, куріння, всі вони об'єднуються терміном «чинники ризику». Всі вони сприяють розвитку атеросклерозу і дисфункції ендотелію (перш за все порушення секреції азоту оксиду та інших вазодилататорів, зниження антиагрегаційних, антипроліферативних властивостей ендотелію).
2. Швидкий шлях (смерть від інфаркту або аритмії).
Провідну роль в порушенні метаболізму азоту оксиду і розвитку ендотеліальної дисфункції грає активація нейрогормональних систем (ренін-ангіотензин-альдостеронової, симпатоадреналової). Активація цих систем викликає зниження експресії азоту оксиду, сприяє гіпертрофії судинної стінки і лівого шлуночка, підвищення проникності судин, розвитку мікроангіопатій, що в свою чергу погіршує дисфункцію ендотелію. Ендотеліальна дисфункція сприяє подальшому розвитку і прогресування атеросклерозу, ішемічної хвороби серця, дестабілізації атеросклеротичної бляшки, підвищенню коагулянтной властивостей крові. В результаті розвиваються інфаркт міокарда з подальшим ремоделюванням міокарда лівого шлуночка і розвитком хронічної серцевої недостатності, яка прогресує і без відповідного лікування призводить до летального результату.
Можлива ланцюг подій включає:
розвиток атеросклерозу коронарних артерій - ІХС - виражена дисфункція ендотелію - коронарний тромбоз - гострий інфаркт міокарда - фатальна аритмія - смерть хворого.
Можливий і інший варіант розвитку подій після гострого інфаркту міокарда:
розвиток вогнища некрозу - процеси глибокого сну в міокарді - ремоделирование лівого шлуночка - хронічна серцева недостатність - смерть.
3. Довгий шлях (хронічна серцева недостаточноть, ураження органів-мішеней).
При артеріальній гіпертензії схема серцево-судинного континууму виглядає наступним чином:
артеріальна гіпертензія - активація нейрогормонів і ендотеліальна дисфункція - гіпертрофія лівого шлуночка і судинних стінок -ремоделірованіе лівого шлуночка, артерій - хронічна серцева недостатність - смерть.
Необхідною стадією розвитку серцево-судинного континууму є ремоделирование лівого шлуночка. Ішемічна хвороба серця може привести до розвитку ішемічної кардіоміопатії в зв'язку з рецидивуючими епізодами ішемії міокарда, станом глибокого сну в певних ділянках міокарда, перенесеними інфарктами міокарда, наявністю вогнищ постінфарктного кардіосклерозу. В подальшому розвивається ремоделирование міокарда та хронічна серцева недостатність.
Артеріальна гіпертензія також призводить до ремоделювання серця з подальшим розвитком хронічної серцевої недостатності. Слід ще раз підкреслити, що ключовими етапами розвитку серцево-судинного континууму є активація нейрогормональних систем, дисфункція ендотелію, ремоделювання міокарда.
Порочне коло в серцево-судинному континуумі.
У 2001 р AM Dart і BA Kingwell описали другий ( «патофізіологічний») континуум, який представляє собою порочне коло, що стартує з етапу пошкодження ендотелію судин і його дисфункції - цієї першопричини атеросклерозу артерій. Далі коло замикається за допомогою підвищення жорсткості стінок резистивних судин, що веде до прискорення пульсової хвилі і підвищення пульсового тиску, а також тиску крові в аорті. В результаті дисфункція ендотелію прогресує, підвищується ризик атеротромботичних ускладнень.
За цією моделлю артеріальна гіпертензія є ключовим фактором прискорення атеросклеротичного процесу і появи коронарної хвороби серця. Остання супроводжується ішемічним пошкодженням міокарда аж до розвитку ІМ і дисфункції серцевого м'яза.
У хворих на артеріальну гіпертензію серце змушене адаптуватися до умов роботи проти високого опору периферичних судин, які у відповідь на підвищення артеріального тиску спазмируются. Рано чи пізно стінка лівого шлуночка серця потовщується, що на перших порах є результатом його адаптації. Згодом в гіпертрофованих кардіоміоцитах (КМЦ) з'являються дегенеративні зміни, в інтерстиціальних просторах накопичується колаген. Вже на ранніх етапах артеріальної гіпертензії формуються гіпертрофія лівого шлуночка (ГЛШ) і діастолічна дисфункція лівого шлуночка (ДД ЛШ).
Навіть м'яка артеріальна гіпертензія збільшує ризик появи ГЛШ в 2-3 рази - цього фактор ризику виникнення інфаркту міокарда та шлуночкових аритмій. Виникнення дисфункції ендотелію судин в умовах окисного стресу сприяє прискореному прогресуванню атеросклеротичного процесу в судинах, в тому числі і коронарних. Це створює загрозу ішемії міокарда і підвищує ризик виникнення ІМ, чому сприяє зниження перфузії м'яза лівого шлуночка внаслідок наявності його гіпертрофії.
Якщо дисфункція діастоли лівого шлуночка є результатом його навантаження високим опором, то дисфункція систоли лівого шлуночка формується внаслідок перевантаження об'ємом. Зниження перфузії тканин кров'ю супроводжується компенсаторною активацією нейроендокринних систем, перш за все симпатоадреналової (САС) і РААС.
Гіперактивація останніх прискорює процес прогресування хронічної серцевої недостатності. Зауважимо, що систолічна дисфункція лівого шлуночка зустрічається у 2% населення, у 50% хворих вона протікає безсимптомно, пацієнти не лікуються, що погіршує прогноз їхнього життя.
При формуванні діастолічної дисфункції лівого шлуночка, коли знижується коронарний резерв і можуть з'являтися різного роду аритмії, ситуація ще оборотна. З етапу виникнення систолічної дисфункції лівого шлуночка ремоделювання серцевого м'яза набуває незворотного характеру.
Фактори ризику.
Чим більше факторів ризику, тим швидше розвиваються події у конкретного пацієнта. Сучасні рекомендації по діагностиці та лікуванню серцево-судинних захворювань (ССЗ) приділяють велику увагу виявленню та корекції факторів ризику (ФР) розвитку патологій серцево-судинної системи (ССС). Ці ФР багато в чому універсальні, тобто характерні для більшості ССЗ, і добре відомі. В даний час ФР поділяють на: «модифікуються» - ожиріння, рівень холестерину, рівень артеріального тиску, наявність НТГ або ЦД 2 типу, куріння; «Немодіфіціруемих» - вік, стать, расова приналежність, обтяжений сімейний анамнез; «М'які» ФР - низький рівень ЛПВЩ, α-ліпопротеїну і тканинного активатора плазміногену-1, високий рівень С-реактивного протеїну, гомоцистеїну, сечової кислоти.
Кожен ФР має свою питому вагу в ймовірності розвитку того чи іншого захворювання серцево-судинної системи. При цьому спільне вплив декількох ФР на одного пацієнта сприяє суттєвому збільшенню ризику розвитку серцево-судинних ускладнень (ССО).
Основні ФР, такі як ожиріння, АГ, СД, атерогенная дислипидемия, являють собою початковий етап в «сердечно-судинному континуумі» - в безперервній послідовності патофізіологічних подій, що призводять до прогресуючого пошкодження клітин різних органів, зокрема, до поразки артеріальної стінки (ремоделювання) і в кінцевому підсумку клінічними проявами ССЗ.
Більшість забезпечених людей, особливо в великих містах цивілізованих країн, прагнуть відповідати сучасним стереотипам людської краси і використовують всі доступні методи збереження і підтримання «вічної молодості». Це найбільш актуально серед молодих людей репродуктивного віку, коли немає ще серйозних хронічних захворювань і питання здоров'я, як такого, їх мало турбують, але є бажання гідно виглядати, щоб знайти престижну роботу, придбати супутника життя, обзавестися сім'єю, словом, бути в соціумі.
Коли до 50-60 років життя, а часом і раніше, виникають серйозні проблеми зі здоров'ям (АГ, ІХС, СД, захворювання суглобів, гормональні порушення та ін.), То супутнє ожиріння, якщо воно має місце, йде як би на другий план . Тоді вся увага в лікуванні направлено на усунення виниклих недуг, при цьому не береться до виду, що їх причиною, можливо, є саме надлишкове відкладення вісцеральної жирової тканини. Ще раз прочитайте цю пропозицію. Вісцеральної жирової тканини, яка виділяє запальні цитокіни!
запальні цитокіни
Жирова тканина - не просто пасивний накопичувач жиру - «акумулятор енергії»: вона є активним ауто-, пара- і ендокринною органом, секретуються в кровотік різні біологічно активні сполуки пептидної і непептідние природи, які відіграють важливу роль в гомеокінеза різних систем, в тому числі і серцево-судинної системи. Адипоцити - функціональні одиниці жирової тканини, є джерелом фактора некрозу пухлини-альфа (ФНП-α), інгібітора активатора плазміногену-1 (ІАП-1), інтерлейкіну-6 (ІЛ-6), лептину, ангіотензиногена, інсуліноподібний фактор росту-1 ( ІФР-1).
Підвищений рівень сечової кислоти
У той же час є невелика кількість робіт, присвячених клінічним і прогностическому значенням гіперурикемії при хронічній серцевій недостатності, хоча ця патологія залишається однією з несприятливих в плані прогнозу в ряду серцево-судинних захворювань. Гіперурикемія розглядається як частина серцево-судинного континууму, як фактор ризику розвитку хронічної серцевої недостатності і маркер її несприятливого перебігу.
інсулінорезистентність
Розвиток серцево-судинних захворювань у осіб зі стійкістю до інсуліну - процес прогресуючий, що характеризується ранньої дисфункцією ендотелію і судинних запаленням, провідним до залучення моноцитів, трансформацією їх в пінисті клітини з утворенням жирових смужок. Через багато років, це веде до зростання атеросклеротичних бляшок, що, при наявності загального провоспалительного фону, виражається в нестабільності і розриві бляшки з окклюзірующего тромбозом. Атероми у осіб з цукровим діабетом мають біль-шиї вміст жиру, в більшій мірі запально змінені і демонструють більш високий ризик тромбоутворення, ніж у осіб без діабету. Ці зміни відбуваються протягом 20-30 років.

