Стаття опублікована на с. 8-14
Остеоартрит (ОА) - одне з найпоширеніших ревматичних захворювань, клінічні симптоми якого спостерігаються більш ніж у 20% населення земної кулі [6]. ОА зустрічається у кожного третього пацієнта віком від 45 до 64 років і у 60-70% хворих старше 65 років [11]. ОА значно погіршує якість життя хворих і є однією з основних причин виникнення тимчасової та стійкої втрати працездатності. Значне збільшення частоти даного захворювання обумовлено перш за все швидким старінням популяцій і пандемією ожиріння [4], тому ОА в даний час стає однією з основних проблем охорони здоров'я практично у всіх країнах. Прогнозують, що до 2020 року поширеність ОА в популяціях може досягти 57%, при цьому істотно збільшуються і витрати на лікування [10]. Добре відомо, що всі ревматичні захворювання мають високу коморбидность насамперед з серцево-судинною патологією. Підвищення кардіоваскулярного ризику описано у пацієнтів із запальними артропатиями і системними захворюваннями сполучної тканини. Встановлено, що наявність двох і більше припухлих суглобів є предиктором серцево-судинної смертності незалежно від інших факторів ризику [15]. У багатьох дослідженнях продемонстровано, що пацієнти з ОА мають значно вищий ризик розвитку коморбідних захворювань, що не страждають ОА [20]. U. Kadam і співавт. (2004) в 18-місячному дослідженні за участю тисяча двадцять шість пацієнтів з ОА у віці старше 50 років виявили чіткий взаємозв'язок між числом хвороб (morbidity counts) і фізичної функцією у цих пацієнтів. У більшості пацієнтів з ОА був високий morbidity counts (більше 5 хвороб) - 49%, 28% пацієнтів мали середній morbidity counts (3-4 хвороби), у 25% був низький morbidity counts (1-2 хвороби), і ОА без супутньої патології виявлено лише у 3,7% хворих [16]. Крім того, ОА асоційований з підвищеним ризиком смертності, а основними факторами ризику є вік, тяжкість захворювання, вираженість больового синдрому і наявність поліморбідних станів [10]. Недарма сьогодні ОА визначають як групу гетерогенних захворювань зі схожими прогресуючими морфологічними змінами тканин суглоба (хряща, субхондральної кістки, синовіальної оболонки, зв'язок, капсули, навколосуглобових м'язів), що приводять до зниження функціональної активності хворого і дестабілізації коморбідних станів [5, 9, 10]. Взаємозв'язку ОА, хронічного больового синдрому і кардіоваскулярної патології схематично представлені на рис. 1.
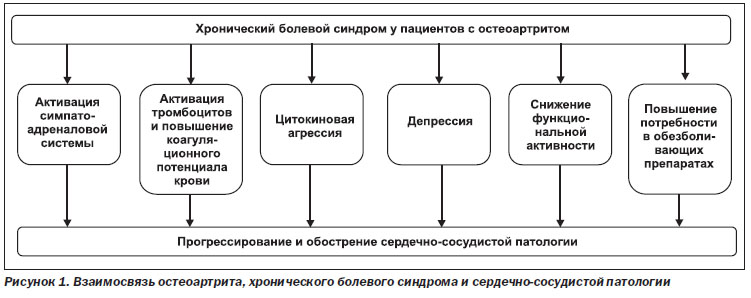
На сьогоднішній день існує безліч доказів того, що ОА - не просто захворювання, пов'язане з порушеннями морфофункціонального стану суглобів, а порушення обміну речовин, при якому розвиваються метаболічні розлади, що сприяють виникненню і прогресу системного патологічного процесу та підтримання низкоуровневого запалення в тканинах. Таким чином, розвиток ОА патогенетично пов'язано не тільки з ожирінням, старінням і травмою, але і з іншими факторами кардіоваскулярного ризику: цукровий діабет, інсулінорезистентністю та дисліпідемією [4, 7].
Існує кілька механізмів розвитку коморбидности [8]. Одним із шляхів розвитку можна вважати появу групи захворювань, об'єднаних одним патогенетичниммеханізмом, наприклад атеросклероз і пов'язані з ним захворювання. Інший шлях розвитку коморбидности - поступове накопичення хвороб через причинно-наслідкового трансформації. Третій шлях - ятрогенний, коли тривале застосування медикаментозних препаратів призводить до виникнення побічних ефектів, що переростають в самостійні нозологічні форми (наприклад, НПЗП-гастропатія при прийомі нестероїдних протизапальних препаратів (НПЗП) або глюкокортикоид-індукований остеопороз при їх тривалому застосуванні). Цей механізм є надзвичайно важливим для ревматологічних хворих. Четвертий вид коморбидности - наявність поєднання різних захворювань з різним ЕТІОПАТОГЕНЕЗ, що ускладнюють перебіг одне одного. Аналіз механізмів розвитку коморбидности при ОА дозволяє акцентувати все 4 шляху як найважливіші в формуванні поліморбідності і підвищення ризику передчасної смерті.
У хворих c ОА в поєднанні з метаболічним синдромом були встановлені значні порушення ліпідного обміну, зростання активності оксидативного стресу, що сприяло деградації сполучнотканинних структур організму. У хворих ОА є підвищений ризик розвитку кардіоваскулярних патологій, який збільшується під час лікування НПЗП при наявності інших факторів - вікових змін, ожиріння та артеріальної гіпертензії. Також у хворих, які страждають ОА, були виявлені пошкодження ендотелію і порушення його функцій - зниження антітромбогенной активності судинної стінки, підвищення пружності артерій, вираженість яких зростає зі збільшенням тривалості захворювання [1, 7]. Супутні ОА захворювання, такі як діабет, онкологічні, серцево-судинні та гастроентерологічні захворювання, обтяжують стан хворих і поряд зі зниженням рухової активності призводять до високого ризику смертності в порівнянні з населенням в цілому незалежно від віку [19]. Таким чином, отримані і накопичені на сьогоднішній день дані літератури дозволяють розглядати ОА як проблему власне системної метаболічної хвороби по суті, але в той же час як проблему поліморбідності, що набуває вже і прогностичний характер [9].
Минулі десятиліття ознаменувалися новим концептуальним підходом щодо патогенезу ОА, який розглядає дане захворювання не тільки як локальну патологію суглобів, а й як цілісний процес, який стосується численні ланки гомеостазу [7]. Різноманіття форм і висока частота супутньої патології у хворих ОА диктують необхідність їх врахування при виробленні тактики лікування суглобів. Часта асоціація ОА з літнім віком та високий індекс коморбідності припускають індивідуальний підхід до лікування таких пацієнтів з корекцією загальної терапії. Наявність супутніх захворювань при ОА вимагає зваженого підходу до призначення лікарських препаратів, щоб уникнути фармакологічного взаємодії і прояви побічних реакцій.
В оновлених рекомендаціях OARSI, опублікованих навесні 2014 р робочою групою експертів робиться наголос на необхідності персоніфікованого підходу до терапії ОА [18]. Такий підхід реалізує один з головних принципів медицини - лікувати не хворобу, а конкретної людини. Сучасна парадигма лікування ОА спрямована на зменшення запалення і інтенсивності больового синдрому, уповільнення прогресування захворювання, поліпшення суглобової функції і, як наслідок, підвищення якості життя хворих, що передбачає раннє і тривале призначення симптом-модифікуючих препаратів уповільненої дії, які не тільки впливають на запалення і біль, але і здатні сповільнити прогресування захворювання, тобто виявляють структурно-модифікуючий дію. Переважання в структурі пацієнтів з ОА осіб похилого віку, наявність коморбідної патології, необхідність тривалого прийому препаратів обумовлюють високі вимоги до безпеки лікарських засобів, що використовуються при ОА.
Серед симптом-модифікуючих препаратів особливий інтерес представляє препарат Піаскледін 300, по-перше завдяки своєму рослинному походженню, а по-друге - значущою антіцітокіновой активності [2]. Піаскледін 300 (неомиляемие з'єднання авокадо і сої - ASU) - оригінальний французький препарат класу SYSADOA, до складу якого входять фітостероли і жирні кислоти, отримані в результаті гідролізу масел авокадо і соєвих бобів методом молекулярної дистиляції в пропорції 1: 2 [2]. На сьогоднішній день доведено, що основні симптом- і структурно-модифікуючі властивості Піаскледіна при ОА обумовлені його унікальним впливом на експресію цитокінів [3, 14]. Препарат пригнічує інтерлейкін-1 (ІЛ-1) - головний патогенетичний фактор розвитку і прогресування ОА, запобігаючи його патологічне вплив на хондроцити та синовіоцити. Піаскледін пригнічує ІЛ-1β-стимульований синтез матриксних металопротеїназ (ММП) хондроцітамі, експресію ІЛ-6 та ІЛ-8, а також простагландину Е2, обумовлює як антикатаболическое вплив на матрикс хряща, так і гальмування вторинного запалення в тканинах суглоба, а саме в синовіальній оболонці, ентезісов, субхондральної кістки і безпосередньо в гиалиновом хрящі [1, 12, 14]. Препарат підвищує експресію трансформують факторів зростання β1 і β2, а також інгібітора плазміногену-1 (PAI-1).
Трансформують фактори росту активно впливають на синтез макромолекул міжклітинної речовини суглобового хряща - протеогліканів і колагену II типу. ТФР-β надає істотний анаболічний ефект і є одним з найпотужніших стимуляторів синтезу матриксу суглобового хряща, одночасно він здатний пригнічувати експресію рецепторів, чутливих до ІЛ-1 [3]. Дослідники припускають, що Піаскледін може змінювати метаболічні процеси в остеоартрозном хрящі шляхом гальмування деградації суглобового хряща і сприяння репаративну процесам [14].
З урахуванням представлених патогенетичних переваг неомильних з'єднань авокадо і сої представляємо клінічні випадки успішного лікування пацієнтів з ОА і коморбидной патологією з використанням індивідуального підходу до пацієнта і оцінкою несприятливих факторів прогресування ОА і супутніх захворювань.
Клінічне спостереження 1. Пацієнт С., 67 років, пенсіонер. При зверненні до ревматолога - скарги на болі в колінних суглобах, особливо в другій половині дня і після фізичного навантаження, труднощі при тривалій ходьбі, підйомах / спусках по сходах, а також періодичне припухання суглобів, що супроводжується випотом і почервонінням області суглоба. Болі в колінних суглобах турбують приблизно 7 років, в динаміці наростають, останнім часом набули сталого характеру, однак пацієнт комплексну терапію остеоартриту не отримував, періодично (без призначення лікаря) брав НПЗП для купірування больового синдрому.
Під час обстеження виявлено дефигурация колінних суглобів за рахунок незначної припухлості, зміна осі з формуванням варусной деформації; болючість при пальпації колінних суглобів, особливо з медіальної сторони; локально температура над суглобами не підвищена; обмеження розгинання і згинання, що супроводжується больовим синдромом. Інші суглобові групи не змінені.
При рентгенографічних обстеженні встановлено діагноз двостороннього гонартроза, праворуч - II стадія, зліва - III стадія: виявляються нерівномірне звуження суглобової щілини, найбільш виражене в медіальних відділах, виражений субхондральний склероз, крайові кісткові розростання. При ультразвуковому дослідженні визуализирован синовит правого колінного суглоба з незначною кількістю рідини і наявністю кісти Бейкера. Загальний аналіз крові: еритроцити - 3,78 × 1012 / л, гемоглобін - 142 г / л, лейкоцити - 5,5 × 109 / л, тромбоцити - 367 × 109 / л, паличкоядерні - 2%, сегментоядерні - 67%, еозинофіли - 1%, лімфоцити - 24%, моноцити - 6%, ШОЕ - 8 мм / год. Ревматоїдний фактор негативний, С-реактивний білок (кількісно) - 12,25 мг / л. Біохімічний аналіз крові: загальний білок - 72 г / л, сечовина - 7,6 ммоль / л, креатинін - 102 мкмоль / л, сечова кислота - 386 мкмоль / л, загальний холестерин - 7,2 ммоль / л, тригліцериди - 3, 18 ммоль / л, холестерин ЛПВЩ - 0,96 ммоль / л, холестерин ЛПНЩ - 4,76 ммоль / л, холестерин ЛПДНЩ - 1,78 ммоль / л, загальний білірубін - 17,7 мкмоль / л, АлАТ - 18 од / л, АсАТ - 22 од / л, КФК - 104 од / л, глюкоза крові - 5,2 ммоль / л. Протромбіновий індекс - 102%, фібрин - 5,22 г / л.
Клінічна картина, інструментальні та лабораторні дані вказували на діагноз остеоартриту, який і був виставлений пацієнтові. Однак при більш детальному опитуванні та обстеженні було встановлено клінічно значуща супутня кардіальна патологія, що також вимагало призначення відповідного лікування і обліку цих даних при призначенні терапії ОА.
Крім суглобових скарг пацієнт пред'являв скарги на підвищення артеріального тиску, його нестабільність, часті болі голови і періодичні запаморочення, перебої в роботі серця, задишку при незначному фізичному навантаженні. Було зафіксовано кілька гіпертонічних кризів, які були успішно куповані, однак пацієнт не приймав постійну антигіпертензивну терапію. Також протягом останніх кількох років пацієнт відзначає постійні перебої в роботі серця, однак ЕКГ не проводилася. При об'єктивному обстеженні: пацієнт підвищеної вгодованості, ожиріння III ст., ІМТ = 36,4 кг / м2. Шкірні покриви блідо-рожеві, без патологічних висипань. Лімфатичні вузли не збільшені. Щитовидна залоза не збільшена, безболісна. У легенях вислуховується везикулярне дихання, ЧД 18 / хв. Межі серця розширені вліво. Серцеві тони аритмічний, зниженою звучності, акцент II тону на аорті. ЧСС - 85-74-58-96 / хв. ДП - 7 / хв. АТ - 170/100 мм рт.ст. Живіт збільшений в об'ємі за рахунок підшкірно-жирового шару, пальпація внутрішніх органів істотно ускладнена. Перкуторно печінку по краю реберної дуги. Сечовипусканнявільне. Пастозность нижніх кінцівок до нижньої третини гомілки.
Пацієнту були проведені додаткові дослідження: холтерівське моніторування ритму серця, ЕКГ, ехокардіографія (ЕхоКГ). Контроль АТ виявив його стійке підвищення до 160/95 мм рт.ст. і вище; на ЕКГ зареєстрована фібриляція передсердь, переважно еусістоліческій варіант.
Ехокардіографія: КДР 5,4 см (норма <5,5 см); КСР 3,9 см (норма <3,8 см); КДО 139 мл (норма <160 мл); КСВ 67 мл (норма <80 мл); ФВ 52%,% С 27%, УО 72 мл, МО 5,5 л / хв. Аорта ущільнена, АТ 3,6 см (норма <3,7), розкриття 1,8; мітральний клапан - стулки не змінені; праве передсердя збільшено, 4,3 × 6,4 см; порожнину правого шлуночка розширена, ПЗР 3,2 см (<2,6); ліве передсердя збільшено, 4,9 × 6,9 см (<4,0); лівий шлуночок - порожнина не розширена. ІПП 1,99; ІПЖ 1,48; ИЛП 2,27; ІЛЖ 2,5. Товщина міжшлуночкової перегородки - 1,4 см, екскурсія - 0,7 см; товщина задньої стінки лівого шлуночка - 1,3 см, екскурсія - 0,9 см. Зони гіпо, а-, дискінезії не встановлені. Тиск на аортальному клапані 12 мм рт.ст., тиск на легеневої артерії 6,0 мм рт.ст.
Висновок: аортосклероз. Помірні склеродегенератівние зміни стулок аортального клапана. Регургітація на аортальному клапані мінімальна, на мітральному клапані - ІІІ ст., На трикуспідального клапані - ІІ-ІІІ ст. Помірне розширення порожнин передсердь і правого шлуночка. Помірне потовщення стінок лівого шлуночка. Глобальна скорочувальна функція лівого шлуночка незначно знижена.
Таким чином, у пацієнта діагностовано: остеоартрит, олігоостеоартріт, безузловая форма, двосторонній гонартроз, праворуч - II стадія, зліва - III стадія, ФНС III. Гіпертонічна хвороба II cтадіі, 3-й ступінь, високий додатковий ризик. Гіпертензивне серце (гіпертрофія лівого шлуночка, за даними ЕКГ і ЕхоКГ). ІХС. Дифузний кардіосклероз. Постійна форма фібриляції передсердь, еусістоліческій варіант. СН II А, із збереженою систолічною функцією лівого шлуночка (ФВ - 52%), ФК III за NYHA. Синдром гіперліпідемії і дисліпідемії. Ожиріння III ст.
З огляду на серйозну кардіологічну патологію, пацієнт був консультував кардіологом, призначено відповідне лікування:
- антикоагулянтна терапія: в зв'язку з постійною формою фібриляції передсердь призначений варфарин в стартовій дозі 2,5 мг під контролем МНО до досягнення цільового рівня 2,0-3,0;
- гиполипидемическая терапія: розувастатин 20 мг 1 раз на день після вечері під контролем показників ліпідограмми;
- сечогінна терапія: торасемід 10 мг 2 рази на тиждень під контролем показників добовогодіурезу, з можливою корекцією дози в майбутньому;
- антигіпертензивна терапія: раміприл 10 мг 1 раз в день + лерканідипін 20 мг 1 раз на день.
Відносно остеоартриту пацієнту була запропонована система модифікації способу життя з поступовим зниженням маси тіла, зменшення калоража їжі, був підібраний оптимальний комплекс фізичних вправ. Вибір симптом-модифікуючої препарату уповільненої дії представляв певні труднощі, оскільки поряд з ефективністю він повинен був бути безпечним у поліморбідних кардіологічного пацієнта, не вступати в лікарський взаємодія з призначеної терапією, перш за все з варфарином, а також по можливості проявляти додаткові позитивні властивості щодо ліпідного обмена.
Був обраний препарат неомильних з'єднань авокадо і сої Піаскледін 300, який рекомендований як симптом-модифікуючої препарату уповільненої дії EULAR і OARSI [2]. Відповідно до рекомендацій OARSI (2010 р), неомиляемие з'єднання авокадо і сої мають розмір клінічного ефекту 0,38 (0,01-0,76), що за клінічною ефективністю щодо симптомів ОА відповідає розміру клінічного ефекту НПЗП. Препарат призначений по 1 капсулі раз на день вранці.
Як відомо, Піаскледін 300 являє собою ліпідні сполуки авокадо і сої в співвідношенні 1: 2, отримані після попереднього гідролізу [3]. Масло авокадо і сої містить біологічно активні компоненти - неомиляемие ліпіди (фітостероли, β-ситостерол, кампестерол і стигмастерол), які проявляють прозапальні, аналгетичні та антиоксидантні властивості, а також мають більш високу ефективність при наявності у пацієнта атеросклерозу [5]. Фітостероли пригнічують абсорбцію холестеролу і перешкоджають його ендогенного біосинтезу. Також було продемонстровано, що фітостероли і частково β-ситостерол є протизапальними агентами з антиоксидантною і аналгетичну активність [13]. Імовірно ці речовини позитивно впливають на перекисне окислення ліпідів, стабілізують мембрани клітин, зменшують патогенну дію активних форм кисню. Саме тому пацієнти з більш високим рівнем окислених ліпопротеїдів низької щільності і антитіл до них більш чутливі до Піаскледіну 300 [5, 10].
Компоненти, що входять до складу Піаскледіна 300, мають натуральне походження, тому їх фармакокінетика не пов'язана з цитохромної системою печінки Р450. Отже, призначення препарату не призведе до зміни метаболізму інших препаратів. Проблема лікарської взаємодії особливо актуальна для варфарину, фармакокінетика якого, як відомо, залежить від прийому великої кількості лікарських препаратів, перш за все антибіотиків (макролідів і цефалоспоринів), гепарину, аміодарону, алопуринолу, циклоспорину та ін. Взаємодія Піаскледіна іварфарину не описано. Таким чином, Піаскледін 300 може претендувати на роль безпечного препарату у поліморбідних пацієнтів. Слід також зазначити, що на відміну від більшості симптоматичних повільнодіючих препаратів Піаскледін 300 має зручну дозування (1 капсула на добу), що, безсумнівно, збільшує прихильність пацієнтів до лікування.
Пацієнту також був призначений НПЗП. З огляду на кардіоваскулярний ризик, був обраний препарат з переважним пригніченням ЦОГ-2 мелоксикам по 15 мг 1 раз на день перорально протягом 2 тижнів з подальшим прийомом на вимогу. Також призначена локальна терапія, рекомендований курс фізіотерапевтичних процедур.
Через 6 міс. була проведена оцінка стану пацієнта. За минулий період він схуд на 8 кг, ІМТ склав 33,7 кг / м2. Пацієнтвідзначав поліпшення загального стану, зменшення вираженості больового синдрому, відсутність епізодів припухания суглобів, збільшення обсягу рухів в суглобах і здатність виконувати фізичне навантаження, яка раніше була недоступна. Також покращився сон, оскільки інтенсивність нічних болів значно знизилася. Симптоми синовіту не визначались, кіста Бейкера значно зменшилася в розмірах. АТ утримувалося на цільовому рівні. На ЕКГ реєструвалася фібриляція передсердь, еусістоліческій варіант. МНО - 2,4. Прояви серцевої недостатності істотно регрессировали і відповідали СН I (ФК II за NYHA). Спостерігалася також позитивна динаміка всіх суглобових показників. Так, початковий рівень болю в колінних суглобах в стані спокою за ВАШ становив 59, через 6 міс. - 37; інтенсивність болю при рухах зменшилася з 74 до 55; тривалість ранкової скутості - з 19 до 11 хв. На початку лікування альгофункціональний індекс Лекена склав 17 балів, через 6 міс. - 14. Зменшення больового синдрому, скутості, поліпшення функціональної активності було також встановлено при аналізі анкети WOMAC. Сумарний індекс WOMAC динамічно змінювався з 1 134 балів до 1006. Важливим критерієм ефективності Піаскледіна стала суб'єктивна оцінка пацієнтом свого стану протягом лікування. Так, пацієнт відзначив загальне поліпшення самопочуття через 2,5 місяці від початку лікування, і це стосувалося поліпшення не тільки стану опорно-рухового апарату, а й симптомів з боку серцево-судинної системи. Важливим є також той факт, що застосування Піаскледіна призвело до зменшення дози, а потім і до повного скасування НПЗП. Зниження дози мелоксикаму (до 7,5 мг) відзначено на 4-му тижні комплексного лікування, а відміна прийому зафіксована на 6-му тижні. В аналізах крові: ШОЕ - 7 мм / год, СРБ - 1,12 мг / л. Значно покращився ліпідний профіль: загальний холестерин - 4,9 ммоль / л, тригліцериди - 1,56 ммоль / л, холестерин ЛПВЩ - 1,12 ммоль / л, холестерин ЛПНЩ - 2,8 ммоль / л, холестерин ЛПДНЩ - 0,67 ммоль / л. Необхідно також відзначити, що за весь період лікування у пацієнта не відзначалося будь-яких побічних реакцій і небажаних ефектів застосування препаратів.
Таким чином, включення препарату Піаскледін 300 в комплексне лікування коморбідних пацієнта з ОА сприяло поліпшенню стану суглобів. Важливим клінічним аспектом дії Піаскледіна також є зниження потреби в НПЗП, позитивний вплив на ліпідний профіль, відсутність взаємодії з антигіпертензивними, гіполіпідемічними і антикоагулянтами, що дає можливість використання даного препарату у коморбідних пацієнтів.
Клінічне спостереження 2. В клініку звернулася пацієнтка Н., 61 рік, зі скаргами на виражені болі в суглобах верхніх і нижніх кінцівок, які турбують переважно в другій половині дня і вночі, ранкову скутість і тугоподвижность суглобів, обмеження рухливості в суглобах, періодичне припухання колінних і гомілковостопних суглобів. Суглобові болі турбують більше 5 років, однак до ревматолога з даною проблемою не зверталася. При зборі анамнезу встановлено, що пацієнтка страждає на цукровий діабет 2-го типу, з приводу якого приймає глімепірид 4 мг вранці і метформін 850 мг двічі на день. Протидіабетичної дієти строго не дотримується. Діагноз діабету встановлено 6 років тому, з цього часу знаходиться на протидіабетичних препаратах. Одночасно спостерігається підвищення тиску до 150-160 / 90 мм рт.ст., що коригує прийомом периндоприлу 4 мг / день.
При огляді: підвищеної вгодованості, ІМТ - 30,7 кг / м2. Шкірні покриви звичайного пофарбування, без патологічних висипань. Лімфатичні вузли, доступні пальпації, не збільшені. У легких при аускультації вислуховується везикулярне дихання, ЧД - 18 / хв. Межі серця незначно розширені вліво. Серцеві тони звучні, ритмічні, акцент II тону над аортою і точкою Боткіна - Ерба. ЧСС - 75 / хв, АТ - 140/90 мм рт.ст. Живіт при пальпації без особливостей. Печінка визначається по краю реберної дуги, край гострий, безболісний, м'яко-еластичний. Селезінка на рівні IX-XI ребра. Відрізки кишечника при пальпації безболісні, рухливі. Сечовипускання не порушено. Незначна гомілок.
Суглоби кистей рук деформовані, визначаються вузлики Гебердена і Бушара на дистальних і проксимальних міжфалангових суглобах, на III пальцях обох рук відзначається незначна болючість цих суглобів при пальпації. Обсяг рухів у дрібних суглобах рук обмежений. Колінні суглоби: визначається припухлість правого колінного суглоба, локальне підвищення температури над суглобом, болючість при пальпації з медіальної боку, пальпується кіста Бейкера в підколінної ямці; лівий суглоб звичайноїконфігурації, без припухлості, температура над суглобом не підвищена, змінена вісь обох суглобів - початкова варусна деформація. Рухи обмежені. Гомілковостопні суглоби припухлі, без локального підвищення температури і явищ запалення, пальпація болюча, рухи болючі і обмежені. У тазостегнових суглобах руху в повному обсязі, безболісні.
Загальний аналіз крові: еритроцити - 4,12 × 1012 / л, гемоглобін - 133 г / л, лейкоцити - 6,2 × 109 / л, тромбоцити - 245 × 109 / л, паличкоядерні - 3%, сегментоядерні - 60%, еозинофіли - 2%, лімфоцити - 33%, моноцити - 2%, ШОЕ - 8 мм / год. Ревматоїдний фактор негативний, С-реактивний білок (кількісно) - 2,25 мг / л. Біохімічний аналіз крові: загальний білок - 65 г / л, сечовина - 8,2 ммоль / л, креатинін - 100 мкмоль / л, загальний холестерин - 7,7 ммоль / л, тригліцериди - 3,25 ммоль / л, холестерин ЛПВЩ - 0,55 ммоль / л, холестерин ЛПНЩ - 4,4 ммоль / л, холестерин ЛПДНЩ - 1,36 ммоль / л, загальний білірубін - 15,5 мкмоль / л, АлАТ - 30 од / л, АЛТ - 36 од / л . Протромбіновий індекс 98%, фібрин - 4,44 г / л. Глікемічний профіль: глюкоза натще - 6,8 ммоль / л, 12:00 - 12,2 ммоль / л, 17:00 - 9,1 ммоль / л, 21:00 - 9,7 ммоль / л.
Проведене ультразвукове та рентгенологічне дослідження дозволило встановити діагноз остеоартриту: правобічний гонартроз II стадії, ускладнений синовітом і кістою Бейкера, лівобічний гонартроз II стадії. При рентгенологічному дослідженні кистей виявлені остеофіти дистальних і проксимальних міжфалангових суглобів, що відповідало III стадії ОА.
Пацієнтка проконсультована ендокринологом і кардіологом, після чого був виставлений комплексний діагноз: остеоартрит, поліостеоартріт, вузликовий варіант, повільно прогресуючий перебіг, стадія III, ФНС I. Реактивний синовіт і кіста Бейкера правого колінного суглоба. Цукровий діабет 2-го типу, протягом середньої тяжкості, стадія субкомпенсації. Гіпертонічна хвороба II стадії, ступінь 3, високий додатковий ризик. Гіпертензивне серце (гіпертрофія лівого шлуночка за даними ЕКГ і ЕхоКГ). СН I. Синдром гіпер- і дисліпідемії.
Таким чином, на прийомі знаходиться коморбідних пацієнтка з ОА, цукровим діабетом, артеріальною гіпертензією та атеросклерозом. Після консультацій фахівців була збільшена доза метформіну до 1000 мг 2 рази на день під час прийому їжі, а також дані чіткі рекомендації по дієті. До комплексної терапії доданий гиполипидемический препарат розувастатин 20 мг 1 раз на день після вечері. Пацієнтка була переведена на комбінований антигіпертензивний препарат периндоприл 4 мг + індапамід 1,25 мг. У зв'язку з больовим синдромом, явищами синовіту правого колінного суглоба був призначений диклофенак 100 мг в ретардной формі, а також місцева терапія гелем з нестероїдних протизапальних препаратом.
Відносно препарату з симптоматичним і хвороба-модифицирующим ефектом на кістково-хрящову тканину вибір був зроблений на користь неомильних з'єднань сої та авокадо (Піаскледін 300). Неомиляемие з'єднання - це технологічна витяжка жирних сполук, що не вступають у реакцію освіти мила при з'єднанні з лугом, в її склад зазвичай входять каротиноїди, токоферол, фітостерини і інші активні речовини. Слід підкреслити, що роль зазначених з'єднань в комплексної стратегії лікування атеросклерозу і інсулінорезистентності незаперечна [17]. У наведеному дослідженні E. Martínez-Abundis з співавт. (2013) вказується роль неомильних з'єднань авокадо і сої в подоланні інсулінорезистентності та маркерів атеросклерозу шляхом зниження концентрації прозапальних цитокінів крові, тобто системного запалення, що лежить в основі формування поліморбідності. Препарат Піаскледін 300 призначений по 1 капсулі 1 раз на день вранці.
Через 6 міс. на повторному прийомі проведена оцінка стану пацієнтки і оцінена ефективність призначення препарату Піаскледін 300. Пацієнтка відзначає суттєве зменшення болю в суглобах, краще переноситься фізичне навантаження, регрессировали симптоми синовіту правого колінного суглоба без повторних епізодів, збільшився обсяг безболісних рухів в суглобах. В цілому пацієнтка відзначає поліпшення свого стану. Показники вуглеводного обміну нормалізування, відзначається компенсація цукрового діабету: показник глікозильованого гемоглобіну 5,8%; глікемічний профіль - 5,5; 7,2; 6,6 ммоль / л. АТ на рівні цільових значень. Показники ліпідного обміну також значно покращилися: загальний холестерин - 4,9 ммоль / л. Лікарських взаємодій і побічних ефектів терапії за час спостереження не відзначалося. НПЗП був скасований на 4-му тижні терапії, місцева терапія триває періодичними курсами по 2 тижні. Альгофункціональний індекс Лекена до лікування склав 20 балів, через 6 міс. - 12. Початковий рівень болю в колінних суглобах в стані спокою за ВАШ становив 63, через 6 міс. - 34; інтенсивність болю при рухах зменшилася з 68 до 46; також значно зменшилася ранкова скутість, складаючи в загальному після лікування близько 6-7 хв. Сумарний індекс WOMAC зменшився з +1268 до 1026 балів. Важливим підсумком лікування була відсутність лікарських взаємодій і побічних ефектів, поліпшення ліпідного і вуглеводного обміну.
Препарат Піаскледін 300 надавав структурно і симптом-модифікуючий вплив на перебіг ОА. Так, позитивний вплив на функціональну активність (здатність хворого пересуватися, виконання певних дій, самообслуговування), зменшення інтенсивності і тривалості скутості в суглобах пацієнти починали відзначати через 3-4 міс. лікування, що було обумовлено структурно-модифікуючих ефектом Піаскледіна. З іншого боку, вплив на больовий синдром, його достовірне зниження в процесі лікування свідчить про наявний протизапальний ефект препарату, що розцінюється як симптом-модифікуючу вплив.
Отже, особливий механізм дії Піаскледіна 300, його висока ефективність, зручність застосування, хороша переносимість, відсутність взаємодії з іншими препаратами, а також можливість застосування у коморбідних пацієнтів дозволяють рекомендувати цей препарат для лікування ОА при поліморбідності як ефективний засіб, що має симптом і структурно модифікують властивості.

