 Сергій Яковлєв: За допомогою одного заборони проблему резистентності до антибіотиків не вирішити. Потрібні системні заходи
Сергій Яковлєв: За допомогою одного заборони проблему резистентності до антибіотиків не вирішити. Потрібні системні заходи
75 років тому ми порушили негласну угоду про співіснування, створивши проти них перше суперзброю - пеніцилін. Приблизно через пару років вони виставили проти нас перших суперсолдатів, які мали стійкістю до антибіотика. З тих пір ситуація тільки ставала гірше. Кожен раз, винаходячи нові ліки, ми одночасно запускали процес селекції мікроорганізмів, здатних захищатися від нього. Сьогодні ВООЗ б'є на сполох: з'явилися мікроби, резистентні до всіх існуючих антибактеріальних препаратів. Чи можна повернути цей процес назад? Мабуть, немає. Однак загальмувати наступ резистентних бактерій нам цілком під силу. Для цього потрібні системні заходи, - вважає віце-президент Альянсу клінічних хіміотерапевтів і мікробіологів Сергій Яковлєв.
- Сергію Володимировичу, коли з'явилася проблема стійкості до антимікробних препаратів?
- Перший антибіотик пеніцилін почали застосовувати в 1941-1942 роках. Уже через два роки, в 1944, виявили стійкі до нього стафілококи. До ванкомицину стафілококи пристосовувалися довше, ніж до пеніциліну, - може, тому, що він менше застосовувався. Але в принципі, як показує практика, у всіх антибіотиків, в тому числі і нових, що з'явилися в останні 15-20 років, термін від введення в медичне вживання до виникнення перших стійких штамів приблизно однаковий: рік-два.
- На чому заснована резистентність? Неправильно застосовуючи антибіотик, ми запускаємо процес селекції мікроорганізмів, які вміють від нього захищатися?
- Відбувається відбір мікроорганізмів, які навчилися виробляти ферменти, що руйнують антибактеріальний препарат. Причому йде селекція не тільки тих бактерій, з якими ми боремося в даний момент. Пресинг антибіотика відчуває вся мікрофлора людини. За даними російського ЦНДІ туберкульозу у 30-40 відсотків людей, які вперше захворіли на туберкульоз, була виявлена стійкість мікобактерій до антибіотиків з групи фторхінолонів - препаратів з групи резерву. Причина в тому, що ці резервні антибіотики щосили використовувалися при банальну застуду. Їх нераціональне застосування гукнулося абсолютно несподівано. Інший приклад. За даними групи професора Сидоренко з НДІ дитячих інфекцій ФМБА, приблизно 20 відсотків кишкових паличок, що викликають банальні інфекції сечовивідних шляхів, сьогодні нечутливі до базових антибіотиків.
- Які мікроби найбільше виробляють резистентність? Раніше пологові будинки закривали через золотистого стафілокока ...
- Серед золотистих стафілококів частка так званих метицилін-резистентних, або стафілококів з множинною лікарською стійкістю, традиційно велика - близько половини. Але по проблемності в Росії зараз на перше місце вийшли два грамнегативних мікроба: клебсієлла і аценетобактер. Клебсієлла взагалі збудник госпітальних інфекцій номер один. Кожна п'ята внутрілікарняна інфекція в світі викликана цією бактерією. І майже всі характеризуються або полірезистентністю, або надзвичайної резистентністю, тобто, зберігають чутливість до одного, максимум - двох антибіотиків.
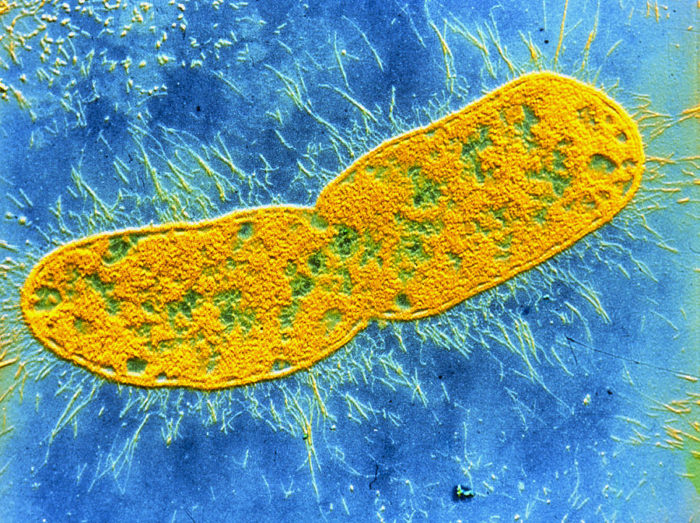
Клебсієлла - збудник госпітальних інфекцій номер один. Кожна п'ята внутрілікарняна інфекція в світі викликана цією бактерією.
- Це та сама клебсієлла, яка зазвичай живе у людини в кишечнику?
- клебсієл, яку виявляють при госпітальних інфекціях, вийшла за межі кишечника і знайшла в стаціонарі нову екологічну нішу. Більш того: в 2005-2008 році з'явилися клебсієлла і аценетобактер зі стійкістю до карбапенемам: бета-лактамних антибіотиків, які довго розцінювалися лікарями як засіб останньої надії. Через резистентності вони перестали бути антибіотиками резерву, що рятують життя. Є хворі, у яких в карті чутливості до антибіотиків суцільні мінуси, які означають резистентність. Звичайно, це не означає, що пацієнт з суперстійкі мікробом неодмінно загине. Але лікувати його складніше і дорожче. І ризик летального результату у нього все одно вище.
- Росздравнадзор зазвичай звітує про 25-30 тисячах випадків госпітальних інфекцій в рік. Це реальна цифра?
- Нещодавно ми провели дослідження госпітальних інфекцій в 32 швидкодопомогових лікарнях по всій країні. Це було так зване активне виявлення інфекцій. Дослідник ретельно переглядав історії хвороби всіх пацієнтів, які перебувають у відділенні, на предмет наявності характерних симптомів. Потім визначали мікроорганізми, що стали причиною інфекції. У січні в один день перевірили всі брали участь в дослідженні реанімації від Санкт-Петербурга до Владивостока, потім, в лютому, хірургічні відділення. Потім терапевтичні, урологічні, неврологічні ... Зробили зріз і порахували середню кількість випадків внутрішньолікарняних інфекцій по стаціонарах. Виявилося, що госпітальні інфекції розвиваються у 7,6 відсотків хворих, які перебувають на лікуванні в стаціонарі. Якщо врахувати, що приблизна кількість пролікованих в стаціонарах в Росії становить приблизно 31-32 мільйона пацієнтів, то госпітальних інфекцій у нас повинно бути 2 мільйони 300 тисяч випадків на рік.
палата виживання
- Чим пояснюєте розбіжність з офіційною статистикою?
- Лікарі часто не повідомляють про такі ускладнення. Чи не роблять позначок в історії хвороби, щоб не підпасти під штрафи та інші покарання: у нас до сих прийнято пояснювати госпітальні інфекції виключно антисанітарією. Звичайно, зараз ставлення до цієї проблеми змінюється, але до сих пір є регіони, де простіше не повідомити про госпітальної інфекції, ніж повідомити. Однак, якщо лікар не повідомить про інфекції, то пацієнт не отримає адекватної терапії. Наприклад, перевіряючи чутливість мікроорганізмів до антибіотиків, ми з'ясували, що майже всі вони були стійкі до цефалоспоринів третього покоління. Подивилися, ніж лікували цих пацієнтів. Тими самими препаратами, до яких мікроби були резистентні. Але лікарі змушені були це робити, оскільки без діагнозу «госпітальна інфекція» вони не могли використовувати дорожчий антибіотик, який в цьому випадку треба було застосовувати.
- Легко уявити результат лікування ...
- За нашими даними, тривалість лікування пацієнта при розвитку госпітальної інфекції в середньому збільшується на 50 відсотків, а ризик летального результату - в п'ять разів.
- Який вихід? Запропонувати лікарням інші антибіотики замість тих, що зараз найчастіше застосовують?
- Проблема не в тому, що один антибактеріальний препарат краще, а інший гірше. Ми не можемо вказати в клінічних рекомендаціях, що, припустимо, пневмонію будемо лікувати препаратом А, тому що для нього рівень доказовості найвищий, відповідно, він найефективніший. У кожному місті, в кожній країні, в кожній лікарні свій склад резистентних мікробів. ECDC, Європейський центр з контролю і профілактиці захворювань, публікує на своєму сайті дані стійкості до антибіотиків у різних країнах. Візьмемо пневмокок - часту причину респіраторних інфекцій. Стійкість цього мікроорганізму до макролідних антибіотиків в Швеції, Норвегії, Ісландії становить 1-5 відсотків від усіх штамів. У той час як на півдні Італії і в Іспанії до макролідів стійкі 50-60 відсотків пневмококів. У Росії, на жаль, біда з локальними даними по резистентності, але ті дослідження, які є, теж показують великий розкид. Нещодавно та ж група професора Сидоренко досліджувала резистентність до антибіотиків бета-гемолітичного стрептокока групи А, частої причини дитячих ангін. З'ясувалося, що в Москві стійкість цього мікроорганізму до макролідів склала 5-7 відсотків, а в Іркутську - близько 30.
Антибіотиків обмежать свободу
- Причини відомі?
- В Європі вважається, що головна причина - політика щодо призначення антибіотиків. У північних країнах лікарі та пацієнти більш дисципліновані, а на півдні Італії і в Іспанії вольниця. Якщо ми належимо європейську карту споживання антибіотиків в тоннах на карту стійкості мікроорганізмів, вони співпадуть: там, де використовується більше антибіотиків, більше резистентність до них. Але повний список причин до кінця не відомий. Можливо, грають роль кліматичні відмінності. Можливо - щільність населення. У великих містах стійких штамів завжди більше, ніж в маленьких: для того, щоб мікроорганізми поширювалися, потрібен тісний контакт людей. Ще один фактор, який все більше впливає на картину антибіотикорезистентності, - зростаюча міграція. Величезні пласти населення переміщаються з одного регіону світу в інший. З Москви до Нью-Йорка всього дев'ять годин. А адже саме в Нью-Йорку вперше була виявлена клебсієлла, стійка до карбапенемам. Туреччина, Греція, південь Італії - країни літнього туризму для росіян - лідери по резистентності до карбапенемів. Резистентні мікроби стали для них ендемічними. Відвідуючи ці країни, людина має високий ризик бути колонізована резистентними бактеріями. Вперше на цю проблему звернули увагу в Англії. Дослідники перевірили велику кількість туристів, що повернулися з Індії, в якій вкрай високий рівень стійкості до карбапенемам. З'ясувалося, що у п'яти відсотків туристів в кишечнику виявили клебсієли, стійкі до карбапенемам, яких тоді у Великобританії не було. Ці небезпечні мікроби «жили» в організмі людини приблизно три місяці, потім зникали. Але за цей час він міг передати їх оточуючим. В цьому небезпека резистентних мікробів: поруч можуть виявитися літня людина з ослабленим імунітетом, маленька дитина. І, якщо вони захворіють, антибіотик буде неефективний.
- Так що ж нам робити? Мити руки перед їжею?
- Це вже немало. Ще вчасно вакцинуватися - вірусні інфекції часто запускають бактеріальні. Але, звичайно, перш за все потрібні системні заходи. В кожному регіоні, в кожній області потрібен свій мікробіологічний моніторинг. Хороша мікробіологічна лабораторія коштує недешево. Але треба створювати центральні референсні лабораторії. З клінічними фармакологами в регіонах біда. У Ставропольському краї вийшли з положення. У них при місцевому мінохоронздоров'я є відділ, який займається аналізом динаміки мікробної флори і на підставі цього дає стаціонарах рекомендації - чим правильно лікувати. Але таких прикладів поки одиниці. Страхові компанії повинні доплачувати лікарням за лікування госпітальних інфекцій, якщо вони виникли з об'єктивних причин. А не чинити як зараз - стаціонару компенсують вартість лікування за основним захворюванням, і, навіть якщо пацієнта на 10 днів затримала на ліжку госпітальна пневмонія, викликана суперстійкі мікробом, ні копійкою більше. Потрібно освіту лікарів первинної ланки - як застосовувати антибіотики, де потрібно, де не потрібно. Наступний момент - донести інформацію до пацієнта. Якщо все зробити правильно, можна вплинути на картину резистентності. У Фінляндії, наприклад, був випадок, коли міністерство охорони здоров'я, відстеживши зростання стійкості пиогенного стрептокока до антибіотиків з групи макролідів, запропонувало лікарям тимчасово замінити макролідні антибіотики іншими препаратами. Через деякий час чутливість до макролідів відновилася. Від держави багато залежить. Недарма ООН, піднявши це питання на вересневій генеральній асамблеї, рекомендувала державам позначити відправні точки вирішення проблеми і запланувати конкретні кроки.
- У Росії такі кроки заплановані?
- Я поки не чув.
- А як же заборона на продаж антибіотиків без рецептів, який ось-ось хочуть ввести?
- Боюся, первинну ланку охорони здоров'я не готова до цього. Напевно, доведеться шукати розумний компроміс. Наприклад, недавно в Білорусії посилили контроль за продажем антибіотиків але, щоб не перевантажувати поліклініки, тимчасово залишили у вільному продажу два антибіотики, розвиваючих мінімальну стійкість, - один для респіраторних, інший для урологічних інфекцій. Можливо, за таким же шляхом доведеться піти і нам. Втім, за допомогою одного заборони на вільний продаж антибіотиків проблему резистентності не вирішити. Повторюся: потрібні системні заходи.
про автора
© Алла Астахова.Ru Чи можна повернути цей процес назад?Сергію Володимировичу, коли з'явилася проблема стійкості до антимікробних препаратів?
На чому заснована резистентність?
Неправильно застосовуючи антибіотик, ми запускаємо процес селекції мікроорганізмів, які вміють від нього захищатися?
Які мікроби найбільше виробляють резистентність?
Це та сама клебсієлла, яка зазвичай живе у людини в кишечнику?
Це реальна цифра?
Який вихід?
Запропонувати лікарням інші антибіотики замість тих, що зараз найчастіше застосовують?
Так що ж нам робити?

