- Стовбурові клітини, які не викликають сумнівів у етичності: Нобелівська премія 2012 року
- Ключ до подальшого прогресу - запобігти відторгненню і перетворення в ракові клітини
- Створення юридичної бази допоможе якнайшвидшої реалізації мрії про регенеративної медицини
- Широка сфера просування досліджень і розробок нових методів лікування
- Прогрес в застосуванні iPS-клітин для створення нових ліків
У серпні виповнилося 10 років з часу публікації наукової статті професора Кіотського університету Яманака Сін'я, в якій повідомлялося про створення iPS-клітин (штучному створенні плюрипотентних стовбурових клітин). У 2014 році були проведені клінічні дослідження з трансплантації пацієнтові тканин клітковини, вироблених з iPS-клітин. Надії людей стикаються з завданнями, які вимагають рішення. Проте, триває впевнене просування до створення нових методів лікування.
Ідея регенеративної медицини одночасно стара і нова. Людина здавна мріяв про можливість повернути втрачений зір, силу знерухомлених кінцівках, змусити битися з новою силою зношене серце ... У широкому сенсі до регенеративної медицини можна віднести окуляри і протези, штучні органи та інші замінюють кошти. Метод клітинної терапії, мав на меті вирішити всі ці завдання шляхом пересадки клітин, привернув до себе живе увагу 35 років тому. У 1981 році були отримані ембріональні стовбурові клітини (ES-клітини) з ембріона мишей, а в 1998 році - ES-клітини людини.
Близько 60 трильйонів клітин дорослого організму людини утворюються завдяки багаторазовому поділу, початком якого служить одна-єдина запліднена яйцеклітина. Стовбурові клітини при розподілі здатні не тільки відтворювати самі себе, а й перетворюватися в різні інші типи клітин (тобто мають плюрипотентні). Таким чином з заплідненої яйцеклітини виробляються найрізноманітніші клітини, складові живий організм.
Ембріональні стовбурові клітини отримують з ембріона ранній стадії - всього після 6-7-кратного поділу заплідненої яйцеклітини. Ці володіють властивістю плюріпотентності (здатністю перетворюватися в різноманітні клітини, що формують живий організм) клітини можна розмножувати практично без обмежень. З одного боку, на ES-клітини покладають великі надії як на вихідний клітинний матеріал для регенеративної медицини. У той же час на цьому шляху залишається ряд невирішених завдань. Це і технологія безпечного стимулювання перетворення в необхідний вид клітин, і технологія придушення реакції відторгнення, і, нарешті, саме серйозна перешкода: морально-етична проблема, пов'язана з тим, що матеріал виробляється з запліднених людських яйцеклітин.
В обстановці, коли весь світ займався дослідженнями, прагнучи змусити ембріональні стовбурові клітини перетворюватися потрібним чином в тканини організму, професор Яманака пішов зовсім іншим шляхом, який і привів його до успіху в отриманні плюрипотентних стовбурових клітин, які не поступаються ембріональних стовбурових.
Стовбурові клітини, які не викликають сумнівів у етичності: Нобелівська премія 2012 року
З 24-х генів, часто виявляються в ембріональних стовбурових клітинах, були визначені чотири, які згодом стали називати «генами Яманака» (Oct3 / 4, Sox2, Klf4, c-Myc). При впровадженні цих генів в шкірні клітини мишей з використанням ретровірусу як доставщика генетичного коду (вектора) були отримані плюрипотентні стовбурові клітини, подібні ембріональних стовбурових. У назві клітин - iPS-клітини (induced pluripotent stem cell, «індуковані плюрипотентні стовбурова клітина») - була навмисно використана маленька буква i за аналогією з отримав тоді поширення по всьому світу продуктом фірми Apple - компактним аудіоплеєром iPod.
Детальна техніка отримання, а також склад чотирьох генів були опубліковані в британському науковому журналі Cell від 25 серпня. Але для того, щоб використовувати iPS-клітини при лікуванні людини, потрібно отримати їх з людського матеріалу. У разі ембріональних стовбурових клітин для переходу від мишачого матеріалу до людського знадобилося 17 років. У створенні iPS-клітин людини професор Яманака домігся успіху вже в 2007 році.
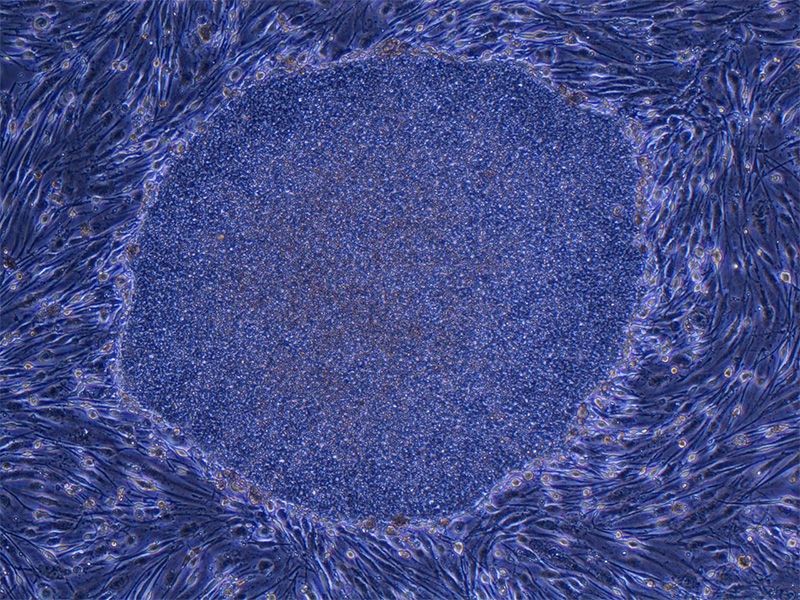 Колонія (група) iPS-клітин людини, вирощених з клітин фібробластів (сполучної тканини). Розмір колонії - приблизно 0,5 мм в діаметрі (фотографія надана професором Яманака Сін'я)
Колонія (група) iPS-клітин людини, вирощених з клітин фібробластів (сполучної тканини). Розмір колонії - приблизно 0,5 мм в діаметрі (фотографія надана професором Яманака Сін'я)
 Професор Яманака Сін'я відповідає на питання на форумі для учнів повних середніх шкіл, який відбувся 4 листопада 2011 року в Токіо (фотографія надана Центром досліджень iPS-клітин Кіотського університету)
Професор Яманака Сін'я відповідає на питання на форумі для учнів повних середніх шкіл, який відбувся 4 листопада 2011 року в Токіо (фотографія надана Центром досліджень iPS-клітин Кіотського університету)
У iPS-клітинах прихований потенціал, який здатний змінити всю клінічну медицину в цілому, не обмежуючись регенеративної медициною. Наприклад, вони породили надію на те, що зіставлення ініціалізованих iPS-клітин людини з клітинами його уражених захворюванням органів дозволить зрозуміти механізм розвитку захворювання і призведе до створення ліків від хвороби. Новина про iPS-клітинах вітали навіть такі противники використання ембріональних стовбурових клітин з етичних міркувань, як президент США Джордж Буш і Папа Римський . Незважаючи на те, що на той момент ці клітини не врятували ні одного хворого, в 2012 року професор Яманака Сін'я був удостоєний Нобелівської премії з фізіології і медицині .
Відкриття iPS-клітин людини дало старт конкуренції на шляху до реалізації мрії про регенеративної медицини.
Первинний метод отримання викликав побоювання у зв'язку з перетворенням клітин в ракові , До того ж ефективність виробництва була вкрай низькою, але завдяки перегляду техніки отримання, а також використовуваних генів, безпеку вдалося підвищити, і в результаті в 2014 році приступили до клінічного випробування. Дванадцятого вересня в лікарні Центру передової медицини Товариства поширення передової медицини (розташований в місті Кобе) в око 70-річної жінки, яка страждає від важкої хвороби зору - дегенерація (ексудативної) жовтої плями - були пересаджені тканини пігментного епітелію сітківки, вирощені за допомогою iPS-клітин з клітин шкіри самої пацієнтки.
Дослідження очолив офтальмолог Такахасі Масаё, керівник проекту Інституту фізико-хімічних досліджень (RIKEN). Основною метою експерименту була оцінка безпеки - вчені мають намір переконатися в приживлюваності клітин, а також в наявності або відсутності перетворень в ракові клітини більш чотирьох років після трансплантації. Через два роки після операції ніяких проблем не виникло. Однак в ході підготовки до запланованої на 2015 рік операції на другому оці пацієнтки в ряді iPS-клітин, вироблених з матеріалу пацієнта, був виявлений ряд генетичних відхилень, в зв'язку з чим від її проведення довелося відмовитися.
Ключ до подальшого прогресу - запобігти відторгненню і перетворення в ракові клітини
Перевага використання матеріалу самого пацієнта для отримання iPS-клітин полягає в тому, що цей підхід дозволяє послабити реакцію відторгнення, від якої залежить доля трансплантації. Однак для першого пацієнта процес отримання з клітин пацієнта iPS-клітин, а також їх подальша культивація і виробництво тканини сітківки при ретельному контролі безпеки зайняли в цілому 11 місяців, а витрати набрякли до сотень мільйонів йен. У зв'язку з цим в наступний раз в RIKEN для отримання клітин сітківки очного яблука, які будуть пересаджені пацієнтові, розраховують скористатися запасом iPS-клітин дослідного центру Кіотського університету. З таким підходом відновити трансплантації планують в 2017 році.
Подібно групам крові, клітини поділяються за типами, утворюючи так звану систему лейкоцитарних антигенів людини (HLA). Подібно до того, як кров першої групи може бути перелита будь-якій людині, існують групи клітин, які не викликають реакції відторгнення при пересадці будь-якій людині. У Кіотському університеті займаються створенням запасу таких iPS-клітин високою універсальності.
 Ємності для зберігання запасу iPS-клітин в науково-виробничому відділі (FiT) Центру досліджень iPS-клітин Кіотського університету (фотографія надана Центром)
Ємності для зберігання запасу iPS-клітин в науково-виробничому відділі (FiT) Центру досліджень iPS-клітин Кіотського університету (фотографія надана Центром)
Навіть при можливому існуванні кількох десятків тисяч типів лейкоцитарних антигенів, що успадкували від батьків лейкоцитарні антигени одного типу люди формують групи за типом АА, BB, CC. І якщо, наприклад, людині з типом АА пересадити клітини від людини типу AB або AC, реакція відторгнення буде мінімальною. Серед японців найбільш часто зустрічаються 75 типів лейкоцитарних антигенів охоплюють 80% населення, а 140 типів покривають 90% жителів. Такі масштаби дозволяють створити в Кіотському університеті достатній запас матеріалу. Заручившись співпрацею Японського Червоного хреста, Банку пуповинної крові та інших організацій, до людей з певними типами лейкоцитарних антигенів звертаються з проханням стати донорами.
У Кіотському університеті з отриманого таким чином донорського матеріалу виготовляють високоякісні iPS-клітини, придатні для лікування. Очікується, що приблизно до кінця 2017 фінансового року буде створено запас, що охоплює по придатності 30-50% японців.
З самого початку найважливішою технологічної завданням було вирішення проблеми перетворення в ракові клітини. Навіть зараз, після переходу до нових методів отримання, не можна стверджувати, що цей ризик зведений до нуля. Коли iPS-клітини вдається стимулювати до повного перетворення в необхідний клітинний матеріал, проблем не виникає. Але якщо в процесі частина клітин залишаються необращённимі, вони можуть привести до розвитку пухлини. Ключем до успіху регенеративної медицини служить розробка методу, який дозволяє або забезпечувати повне преобразовніе, або дає можливість позбуватися від матеріалу, який не відповідає поставленому завданню.
Створення юридичної бази допоможе якнайшвидшої реалізації мрії про регенеративної медицини
На шляху до практичної реалізації методів лікування з використанням iPS-клітин держава надає підтримку, займаючись вирішенням завдань юридичної та іншого характеру. У листопаді 2014 року було внесено поправки в колишній Закон про фармацевтиці. Відносно клітинних тканин і інших «виробів регенеративної медицини» держава підтвердило: в разі, якщо безпеку перевірена, держава дозволяє використовувати такий матеріал як медичний препарат на етапі, коли він вважається ефективним, в обмежені терміни і для обмеженого кола покупців. Що стосується ефективності, то в разі, якщо після закінчення певного терміну продажу вона піддається перевірці, матеріал отримує офіційне затвердження після проходження відповідних обстежень. Якщо за старим законом для отримання дозволу потрібно більше десяти років, то тепер можна очікувати скорочення цього терміну до 2-3 років.
Хоча нове законодавство розглядають як найбільш передове на світовому рівні, в той же час можна стверджувати, що воно є проявом рішучості йти на певний ризик, оскільки Японія визнає кошти регенеративної медицини перш, ніж решта світу.
З іншого боку, новий закон прийнятий і в цілях захисту пацієнтів - щоб запобігти «сіре» (що не потрапляє під дію системи медичного страхування) застосування на свій страх і ризик методів регенеративної медицини, безпеку і ефективність яких ще не визначена.
Широка сфера просування досліджень і розробок нових методів лікування
В даний час дослідження з метою застосування iPS-клітин в різноманітних методах лікування серцевої недостатності, пошкоджень спинного мозку, хвороби Паркінсона і маси інших захворювань наближаються до переходу від випробувань на тваринах до клінічних випробувань на людях.
Декан медичного факультету Університету Кейо Окано Хідеюкі займається переходом до практичної реалізації методу лікування ушкоджень спинного мозку. Оскільки при пошкодженнях спинного мозку в результаті нещасних випадків і травм порушення швидко набуває хронічного характеру, на своєчасне отримання iPS-клітин з власних тканин пацієнта немає часу. Тому в справу вступає згаданий раніше запас iPS-клітин Кіотського університету, які планується звертати в нервові стовбурні клітини. В даний час робота просувається з тим, щоб виконати першу трансплантацію людині вже в 2017 фінансовому році. Це відкриває перспективу використання такого підходу і при лікуванні інсультів.
У той же час професор Осакського університету Сава Йосіюкі веде роботу, метою якої є лікування серцевої недостатності методом пересадки до серця тканини серцевого м'яза, отриманої з iPS-клітин.
У Кіотському університеті професор Такахасі Дзюн займається розробкою методу боротьби з трудноизлечимой хворобою Паркінсона, суть якого полягає в отриманні виробляють допамін нервових клітин з iPS-клітин. Більш того, щоб вирішити проблему нестачі донорів крові в старіючому суспільстві, спільно з Японським товариством Червоного хреста ведеться робота по отриманню з iPS-клітин тромбоцитів і еритроцитів. Просувається і реалізація плану створення методу лікування ракових захворювань за допомогою активізації клітин імунної системи з використанням технології iPS-клітин.
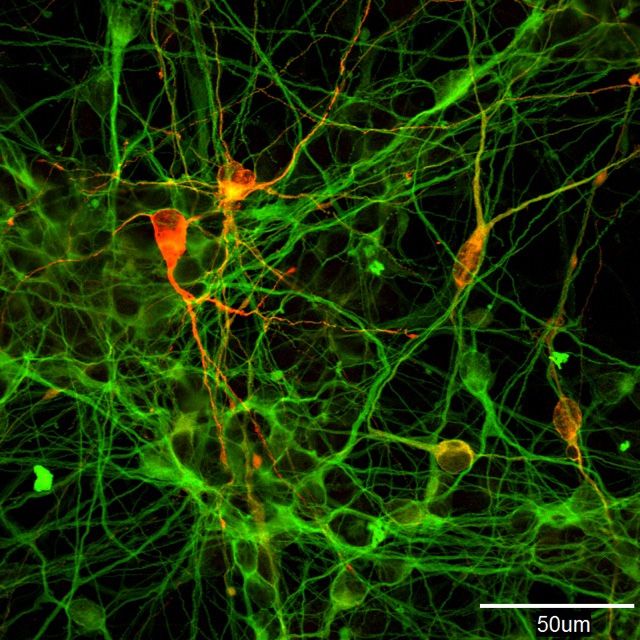 Клітини-виробники допаміну, отримані за допомогою ініціації перетворення iPS-клітин людини (фотографія надана Морідзане Асука з Цетру досліджень iPS-клітин Кіотського університету)
Клітини-виробники допаміну, отримані за допомогою ініціації перетворення iPS-клітин людини (фотографія надана Морідзане Асука з Цетру досліджень iPS-клітин Кіотського університету)
Робляться і спроби створення цілих органів. Професор Танігуті Хідекі з Університету міста Йокогама далеко просунувся в створенні об'ємних елементів печінки з клітин-прекурсорів (клітин, які діляться і перетворюються в клітини організму при його формуванні).
Прогрес в застосуванні iPS-клітин для створення нових ліків
Великі надії з самого початку покладаються і на друге основний напрямок використання - створення нових лікарських препаратів.
Кажуть, що частка речовин, які виявляються придатні до створення ліків, серед інших подібних становить не більше одного на кілька десятків тисяч, при цьому в багатьох випадках розробники стикаються на півдорозі з виникненням важких побічних ефектів, що змушують починати проби з самого початку. iPS-клітини здатні виступати в якості інструменту, за допомогою якого побічні ефекти можна спрогнозувати заздалегідь. Наприклад, скориставшись клітинами печінки, отриманими шляхом перетворення iPS-клітин, можна заздалегідь передбачити печінкову токсичність. Крім того, серед побічних ефектів слід виділити аритмію, яка загрожує самому життю пацієнта. Передбачити цей ефект стає можливим з використанням тканин серцевого м'яза, отриманих перетворенням iPS-клітин.
Великі очікування пов'язані і з областю важко виліковних захворювань. У 2012 році Міністерство освіти, культури, спорту, науки і технологій, а також Міністерство охорони здоров'я, праці і добробуту приступили до реалізації науково-виробничого проекту, спрямованого на боротьбу з важковиліковні захворюваннями, з використанням iPS-клітин. Він полягає в тому, щоб брати у пацієнта з важковиліковним захворюванням клітини організму - шкіри, крові і т. Д., Отримувати в п'яти центрах спільних досліджень, в тому числі в Кіотському університеті, iPS-клітини, змінені захворюванням, і встановлювати природу захворювання, спостерігаючи за їх перетвореннями в хворі тканини, що може привести до створення ліків для лікування хвороби. У співпраці з 50 групами дослідників важко виліковних хвороб при Міністерстві охорони здоров'я, праці та соціального забезпечення участь в проекті беруть 7 фармацевтичних компаній.
Для практичної реалізації методів лікування з використанням iPS-клітин уряд виділяє десятки мільярдів йен, проте все ще залишаються завдання в плані підготовки кадрів. У наукових колах японської регенеративної медицини почала діяти система ліцензування для «лікарів-фахівців регенеративної медицини» і «фахівців за клінічним вирощування клітинних культур». Таким чином, за підготовку кадрів, які володіють технологіями виробництва і обробки клітинних матеріалів, взялися всерйоз.
Якщо вже можна констатувати, що за минуле десятиліття вдалося приступити до клінічних досліджень iPS-клітин, в той же час необхідно визнати, що до того часу, коли ними зможе скористатися будь-який потребує, ще належить пройти довгий шлях. Але вчені з усього світу, на чолі з піонером у цій галузі, професором Яманака Сін'я, вірять в можливості iPS-клітин і не шкодують зусиль в їх дослідженнях, прагнучи збалансувати швидкість і безпеку, ризики і вигоди використання.
Фото до заголовку: дослідник ставить досвід у відкритій лабораторії Центру досліджень iPS-клітин Кіотського університету (фотографія надана Центром)
(Стаття на японській мові опублікована 28 вересня 2016 г.)
